
| A. | 0.lmol的Na2O2含阴阳离子总数为0.4NA | |
| B. | 32g硫与足量金属铜反应转移电子数为NA | |
| C. | 标准状况下,11.2LNO与11.2LO2混合后其原子总数为2NA | |
| D. | 1LpH=1的硫酸溶液中,含有0.2NA个H+ |
分析 A、过氧化钠由2个钠离子和1个过氧根构成;
B、求出硫的物质的量,然后根据硫和铜反应后变为-2价来分析;
C、NO和氧气混合后发生反应,但反应过程中满足原子个数守恒;
D、pH=1的硫酸溶液中,氢离子浓度为0.1mol/L.
解答 解:A、过氧化钠由2个钠离子和1个过氧根构成,故0.1mol过氧化钠中含阴阳离子共0.3NA个,故A错误;
B、32g硫的物质的量为1mol,而硫和铜反应后变为-2价,故1mol硫反应转移2NA个电子,故B错误;
C、NO和氧气混合后发生反应,但反应过程中满足原子个数守恒,标况下11.2LNO和11.2L氧气的物质的量均为0.5mol,而NO和氧气均为双原子分子,故均含1mol原子,混合后原子总数不变,即原子总数为2NA个,故C正确;
D、pH=1的硫酸溶液中,氢离子浓度为0.1mol/L,故1L溶液中含有的氢离子的物质的量为0.1mol,个数为0.1NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.


科目:高中化学 来源: 题型:选择题
 吗丁啉是一种常见的胃药,其有效成分的结构简式如图所示.下列关于该物质的说法中正确的是( )
吗丁啉是一种常见的胃药,其有效成分的结构简式如图所示.下列关于该物质的说法中正确的是( )| A. | 该物质属于芳香烃 | |
| B. | 该物质的相对分子质量很大,属于高分子化合物 | |
| C. | 该物质是一种蛋白质 | |
| D. | 该物质可以发生水解反应和加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | P4和CH4都是正四面体分子且键角都为109o28ˊ | |
| B. | H2O是一种非常稳定的化合物,这是由于氢键所致 | |
| C. | NO3-和CO32-是等电子体,均为平面正三角形结构 | |
| D. | 金属晶体与熔融态的离子晶体导电都是物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸式滴定管和容量瓶在使用前都要用相应溶液润洗 | |
| B. | 常温下,向Fe和Cu中分别加人浓硝酸,可以比较Fe和Cu的金属活动性强弱 | |
| C. | 制取无水MgCl2固体,可将MgCl2溶液置于蒸发皿中加热蒸干 | |
| D. | 分离乙酸乙酯和饱和Na2CO3溶液可用分液的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用丙烷的燃烧反应,可以设计成原电池 | |
| B. | 选用丙烷作燃料,除了环保外,还因为它常温常压下是液态,便于储存 | |
| C. | 火炬燃烧时,存在两种能量转化形式 | |
| D. | C3H8燃烧反应中反应物的键能和大于生成物键能和 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 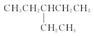 在核磁共振氢谱中有7个吸收峰 在核磁共振氢谱中有7个吸收峰 | |
| B. | 红外光谱图只能确定有机物中所含官能团的种类和数目 | |
| C. | 质谱法不能用于相对分子质量的测定 | |
| D. | 核磁共振氢谱、红外光谱和质谱都可用于分析有机物结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cr的价电子排布式为3d44s2 | |
| B. | 电子式为  可以同时表示羟基和氢氧根离子 可以同时表示羟基和氢氧根离子 | |
| C. | 1s22s22p3和 1s22s22p4能形成AB2型共价化合物 | |
| D. | 基态镁原子核外电子排布图为  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝片与稀盐酸的反应 | B. | Ca(OH)2与NH4Cl的反应 | ||
| C. | 灼热的炭与CO2的反应 | D. | 天然气在氧气中的燃烧反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com