
维生素A对人体,特别是对人的视力有重大作用,其结构简式如图所示:下列关于该化合物的说法正确的是
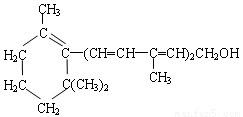
A.维生素A的分子式为C16H25O
B.维生素A含有苯环结构
C.维生素A的一个分子中有3个双键
D.维生素A的分子中含有两种官能团
科目:高中化学 来源:2016届天津市河东区高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
在印染工业中,连二亚硫酸钠(Na2S2O4)因能使染好的布褪色,而使布能重新染色,故而俗称保险粉,其可溶于水,但不溶于甲醇。工业制备流程如下:
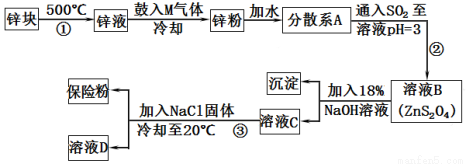
请回答下列问题:
(1)流程①步骤中需在耐高温的坩埚中进行,常用来制做耐高温坩埚的金属氧化物化学式为 。
(2)由锌块制备锌粉的目的是 ;向锌液中鼓入M气体,使液态锌雾化,冷却得到粒度约为180 的锌粉。鼓入气体M为常见的化合物,则M的化学式为 ;分散系A为 (填“溶液”“胶体”或“悬浊液”)。
的锌粉。鼓入气体M为常见的化合物,则M的化学式为 ;分散系A为 (填“溶液”“胶体”或“悬浊液”)。
(3)流程②步骤中的化学方程式为 。
(4)流程③的分离方法步骤为 、洗涤、干燥,洗涤所用试剂是 ;过滤前加入NaCl固体的作用是 。
(5)将等体积0.04 mo1·L-1AgNO3溶液和0.02 mol·L-1碱性Na2S2O4溶液混合,两者恰好完全
反应,反应后溶液中有纳米级的银粉生成,写出反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川市高三4月质检理综化学试卷(解析版) 题型:选择题
下列对有机反应类型的描述不正确的是
A.乙醇使酸性KMnO4溶液褪色,是因为发生了氧化反应
B.将苯加入溴水中,振荡后水层接近无色,是因为发生了取代反应
C.乙烯使溴的四氯化碳溶液褪色,是因为发生了加成反应
D.甲烷与氯气混合,光照一段时间后黄绿色消失,是因为发生了取代反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南嘉积中学高二下期中理科化学试卷(解析版) 题型:填空题
某芳香烃A,其相对分子质量为104,碳的质量分数为92.3%。
(1)A的分子式为_____________;
(2)A与溴的四氯化碳溶液反应的化学方程式为_____________,反应类型是_____________;
(3)一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出此化合物的结构简式_____________;
(4)在一定条件下,由A聚合得到的高分子化合物的结构简式为_____________;
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三下学期考前练习化学试卷(解析版) 题型:填空题
氢能是一种极具发展潜力的清洁能源,硫碘循环制氢主要的热化学方程式为:
Ⅰ.SO2(g)+2H2O(l)+I2(g)=H2SO4 (l)+2HI(g) △H=35.9 kJ/mol
Ⅱ.2H2SO4(l)=2SO2(g)+O2(g)+2H2O(l) △H=470kJ/mol
Ⅲ.2HI(g)=H2(g)+I2(g) △H=14.9kJ/mol
(1)反应2H2(g)+ O2(g)=2H2O(l)的△H= mol·L-1。
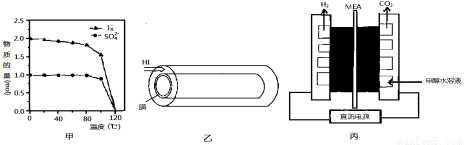
(2)反应Ⅰ在液相中发生称为bensun反应,向水中加入1mol SO2和3mol I2,在不同温度下恰好完全反应生成的n(SO42-)和n(Ix-)的变化见图甲。
①Ix-中x= 。②温度达到120℃时,该反应不发生的原因是 。
(3)反应Ⅲ是在图乙中进行,其中的高分子膜只允许产物通过,高分子膜能使反应程度 ___ (填“增大”、“减小”或“不变”),在该装置中为了进一步增大达平衡时HI的分解率;不考虑温度的影响,还可以采取的措施为 。
(4)图丙是一种制备H2的方法,装置中的MEA为允许质子通过的电解质膜。
①写出阳极电极的反应式: 。
②电解产生的氢气可以用镁铝合金(Mg17Al12)来储存,合金吸氢后得到仅含一种金属的氢化物(其中氢的质量分数为0.077)和一种金属单质,该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三下学期考前练习化学试卷(解析版) 题型:选择题
下列实验操作、现象与结论对应关系正确的是
选项 | 操作 | 现象 | 结论 |
A | 将Fe(NO3)2溶于稀H2SO4后,滴加KSCN溶液 | 溶液变成红色 | Fe(NO3)2中一定含Fe3+ |
B | 从煤油中取出一小块钠,用滤纸擦净表面的煤油,放入无水乙醇中 | 产生气泡 | Na能置换出醇羟基中的氢 |
C | 将某气体通入品红溶液 | 溶液褪色 | 气体一定是SO2 |
D | 向NaAlO2溶液中滴入NaHCO3溶液 | 产生白色沉淀 | AlO2-结合H+的能力比CO3-强 |
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川二中高三三模理综化学试卷(解析版) 题型:实验题
工业废铁屑(含有一些不溶于酸的杂质)为原料生产硫酸钾、过二硫酸铵和氧化铁红颜料,其主要流程如下:
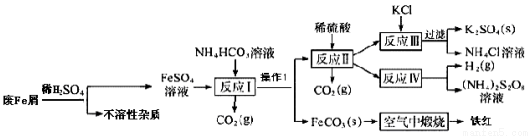
(1)反应I加入NH4HCO3的作用是除去过量的酸,还有一个作用是____________;
(2)反应I需控制反应温度低于35℃,其目的是____________,操作①名称是____________,检验反应Ⅱ溶液中阳离子的方法是____________;
(3)工业生产上常在反应Ⅲ的过程中加入一定量的醇类溶剂,其目的是____________;
(4)己知FeCO3的Ksp=2×10-11,反应I中Fe2+完全沉淀后,溶液中c(CO32-)=____________;
(5)写出FeCO3在空气中锻烧的化学反应方程式____________;
(6) NH4C1溶液显酸性,其浓溶液可用于除去铁锈,其原理是(用离子反应方程式表示)____________。
查看答案和解析>>
科目:高中化学 来源:2016届宁夏石嘴山三中高三下四模理综化学试卷(解析版) 题型:选择题
某溶液除水电离出的OH﹣、H+之外仅含Fe2+、Na+、Al3+、Ba2+、NO3-、SO42-、Cl﹣中的4种,这4种离子的物质的量均为0.1mol.若向该溶液中加入少量稀硫酸,无沉淀生成但有气泡产生.下列说法错误的是
A.该溶液中肯定不含Ba2+
B.该溶液中除H+、0H﹣之外所含离子是Fe2+、Na+、NO3-、SO42-
C.若向该溶液中加入过量的稀硫酸,溶液中的阴离子会减少一种
D.若向该溶液中加入足量NaOH溶液,滤出沉淀,洗净灼烧后最多能得8.0g 固体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com