
���� X��Y��Z��Q��R��T�ֱ����ԭ��������������Ķ�����Ԫ�أ�X��Y��Zͬ���������ڣ����ǵ����ʵ����Ԫ�أ���XΪC��YΪN��ZΪO��X��Rͬ�壬��RΪSi��Q��Tԭ�ӵ�����������֮������Rԭ��������������2������Q��Tԭ������������֮��Ϊ8������ԭ����������������T����Ϊ����ɫ���壬��TΪSԪ�أ�QΪMg��U��d��Ԫ�أ�U2+�ĺ�������ܼ���2�ԳɶԵ��ӣ�ԭ����Χ�����Ų�Ϊ3d74s2����UΪCo���ݴ˽��
��� �⣺X��Y��Z��Q��R��T�ֱ����ԭ��������������Ķ�����Ԫ�أ�X��Y��Zͬ���������ڣ����ǵ����ʵ����Ԫ�أ���XΪC��YΪN��ZΪO��X��Rͬ�壬��RΪSi��Q��Tԭ�ӵ�����������֮������Rԭ��������������2������Q��Tԭ������������֮��Ϊ8������ԭ����������������T����Ϊ����ɫ���壬��TΪSԪ�أ�QΪMg��U��d��Ԫ�أ�U2+�ĺ�������ܼ���2�ԳɶԵ��ӣ�ԭ����Χ�����Ų�Ϊ3d74s2����UΪCo��
��1��YΪNԪ�أ���Χ�����Ų�ʽΪ2s22p3������������p�ܼ�������p��Ԫ�أ�QΪMg��ԭ�ӵĺ�������Ų�ʽΪ1s22s22p63s2��
�ʴ�Ϊ��p��1s22s22p63s2��
��2��SO3������Sԭ�ӹµ��Ӷ���Ϊ$\frac{6-2��3}{2}$=0���۲���Ӷ���Ϊ3+0=3������Ϊƽ���������Σ�������������������غϣ����ڷǼ��Է��ӣ�
NO2-������Nԭ�Ӽ۲���Ӷ���Ϊ2+$\frac{5+1-2��2}{2}$=3��VSEPRģ��Ϊƽ�������Σ�
�ʴ���Ϊ���Ǽ��ԣ�ƽ�������Σ�
��3����ԭ�Ӱ뾶С����ԭ�ӣ���Ԫ�طǽ����Ը�ǿ�����⻯���ȶ���H2O��H2S��
�ʴ�Ϊ��H2O����ԭ�Ӱ뾶С����ԭ�ӣ���Ԫ�طǽ����Ը�ǿ����̬�⻯����ȶ��Ժã�
��4��ͨ������£�Co2+����Һ���ȶ�������NH3�γɵ���λ��Ϊ6��������ȴ���ȶ����ڿ������ױ�����Ϊ[Co��NH3��6]3+���÷�Ӧ�����ӷ���ʽ�ǣ�4[Co��NH3��6]2++O2+2H2O�T4[Co��NH3��6]3++4OH-��
�ʴ�Ϊ��4[Co��NH3��6]2++O2+2H2O�T4[Co��NH3��6]3++4OH-��
���� �����Ƕ����ʽṹ�����ʵĿ��飬�漰��������Ų������Ӽ��ԡ��۲���ӶԻ������ۡ������ȣ��ƶ�Ԫ���ǽ���ؼ���ע��Ի���֪ʶ���������գ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϩ�������ӳɣ�1��2-�������飩 | |
| B�� | ��ϩ��ˮ�ӳɣ��Ҵ��� | |
| C�� | �����ʵ����������������ڹ��������·�Ӧ��һ�����飩 | |
| D�� | Һ���뱽���廯����������Ӧ���屽�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬλ�� | B�� | ͬ���칹�� | C�� | ͬ�������� | D�� | ͬ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ӧ��SiO2+Na2CO3$\frac{\underline{\;����\;}}{\;}$Na2SiO3+CO2����˵��H2SiO3�����Դ���H2CO3������ | |
| B�� | ��ΪSO2����Ư���ԣ���������ʹƷ����Һ����ˮ��ɫ | |
| C�� | �����������������ά�������Ļ���ԭ�� | |
| D�� | CO2��CH4��N2���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2.0g D218O�к��е�������ΪNA | |
| B�� | ��״���£�22.4L NH3���Ӻ��е��ӻ������Ϊ4NA | |
| C�� | 78g Na2O2�������������������Ӹ�����Ϊ2NA | |
| D�� | 1mol Fe��ȫ����һ������������Һ�У�ת�Ƶĵ�����һ����3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 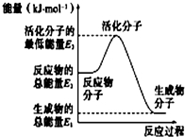 ��Ӧ���е������仯��ͼ��ʾ�����H2=E1-E3 | |
| B�� | H2��ȼ����Ϊ241.8 kJ•mol-1 | |
| C�� | �ɷ�Ӧ��֪���¶�һ���������£���һ�����ܱ�������ͨ��1 mol N2��3 mol H2����Ӧ��ų�������ΪQ1 kJ����ͨ��2 mol N2��6 mol H2��Ӧ��ų�������ΪQ2 kJ����184.8��Q2��2Q1 | |
| D�� | ���Ĵ�������ӦΪ4NH3��g��+5O2��g��=4NO��g��+6H2O��g����H=+906 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��þƬ���� | B�� | ���������� | C�� | ���� | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com