
【题目】研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果。下列表达不正确的是( )
A. 分散质粒子直径与分散系种类:
B. NaOH溶液与CO2反应后溶液中的钠盐:![]()
C. AlCl3 溶液中滴加NaOH溶液后铝的存在形式:
D. Na与O2反应的产物:![]()
【答案】D
【解析】A项正确,根据分散质粒子直径大小,将常见混合物分为溶液、胶体和浊液,分散质粒子直径1小于10-9m的属于溶液,大于10-7m的属于浊液,介于10-9—10-7m之间的属于胶体;B项正确,CO2与碱反应时产物与二者的相对量有关,如:①CO2足量时:CO2+NaOH=NaHCO3②CO2不足时:CO2+2NaOH=Na2CO3+H2O,![]() <1时,只发生反应①,生成NaHCO3,
<1时,只发生反应①,生成NaHCO3,![]() >2时,只发生反应②,生成Na2CO3,1<
>2时,只发生反应②,生成Na2CO3,1<![]() <2时,既有NaHCO3又有Na2CO3;C项正确,可能发生反应为:①Al3++3OH-(少量) =Al(OH)3↓②Al3++4OH-(足量) =AlO2-+H2O,
<2时,既有NaHCO3又有Na2CO3;C项正确,可能发生反应为:①Al3++3OH-(少量) =Al(OH)3↓②Al3++4OH-(足量) =AlO2-+H2O,![]() <3时,只发生①生成Al(OH)3↓,剩余Al3+,
<3时,只发生①生成Al(OH)3↓,剩余Al3+,![]() >4时,只发生反应②生成AlO2-,剩余OH-,3<
>4时,只发生反应②生成AlO2-,剩余OH-,3<![]() <4时,既有Al(OH)3又有AlO2-;D项错误,Na与氧气反应产物与反应条件有关,一般常温生成Na2O,加热生成Na2O2。综上所述,答案选D。
<4时,既有Al(OH)3又有AlO2-;D项错误,Na与氧气反应产物与反应条件有关,一般常温生成Na2O,加热生成Na2O2。综上所述,答案选D。


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】在学习了化学反应速率知识后,某研究性学习小组进行了科学探究活动。
[探究活动一]探究金属与不同酸反应的反应速率:常温下,用经过砂纸打磨的铝片中取两片质量相等、表面积相同的铝片,分别加入到盛有体积相同、c(H+)相同,足量的稀硫酸和稀盐酸溶液的两支试管中,发现铝片在稀盐酸中消失的时间比在稀硫酸中短。
(1)对[探究活动一]实验现象发生的原因,请你帮该研究性学习小组提出两个假设:
假设Ⅰ_______________________________。
假设Ⅱ_______________________________。
并请你设计实验对以上假设进行验证:
验证假设Ⅰ_______________________________。
验证假设Ⅱ_______________________________。
[探究活动二]某小组在实验室测定氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率。
(2)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)2NH3(g)+CO2(g).
实验测得不同温度下的平衡数据列于下表:
温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
①可以判断该分解反应已经达到化学平衡状态的是 .
A.2v(NH3)=v(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0℃时的分解平衡常数: .
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡.若在恒温下压缩容器体积,氨基甲酸铵固体的质量 (填“增加”、“减小”或“不变”).
④氨基甲酸铵分解反应的焓变△H 0,熵变△S 0(填>、<或=).
(3)已知:NH2COONH4+2H2ONH4HCO3+NH3H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如下图所示.
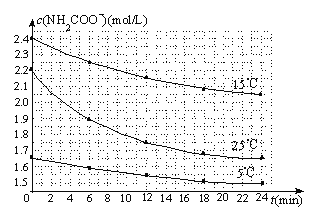
⑤计算25℃时,0~6min氨基甲酸铵水解反应的平均速率: .
⑥根据图中信息,如何说明水解反应速率随温度升高而增大: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施不符合节能减排的是
A.大力发展火力发电,解决电力紧张问题
B.在屋顶安裝太阳能热水器为居民提供生活用热水
C.用石灰对煤燃烧后形成的烟气脱硫,并回收石膏
D.用杂草、生活垃圾等有机废弃物在沼气池中发酵产生沼气,作家庭燃气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2015·上海]下列有关物质性质的比较,错误的是
A.溶解度:小苏打<苏打 B.密度:溴乙烷>水
C.硬度:晶体硅<金刚石 D.碳碳键键长:乙烯>苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S水溶液中存在电离平衡H2S![]() H++HS-和HS-
H++HS-和HS-![]() H++S2-,若向H2S溶液中
H++S2-,若向H2S溶液中
A.加水,平衡向右移动,溶液中氢离子浓度增大
B.通入过量SO2气体,平衡向左移动,溶液pH增大
C.滴加新制氯水,平衡向左移动,溶液pH减小
D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2016·新课标全国Ⅲ]化学在生活中有着广泛的应用,下列对应关系错误的是
选项 | 化学性质 | 实际应用 |
A | Al2(SO4)3和小苏打反应 | 泡沫灭火器灭火 |
B | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板 |
C | 次氯酸盐具有氧化性 | 漂白粉漂白织物 |
D | HF与SiO2反应 | 氢氟酸在玻璃器皿上刻蚀标记 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的Mg、Zn、Al混合物与足量稀H2SO4反应,生成H22.8L(标准状况),原混合物质量可能是( )
A. 2g B. 4g C. 10g D. 12g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从2L1mol/L NaOH溶液中取出100mL,下列关于这100mL溶液的叙述错误的是( )
A.浓度为0.1mol/L B.浓度为1mol/L
C.含NaOH 4g D.含NaOH 0.1mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com