
 糠醛(
糠醛(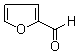 )可与新制含有NaOH的Cu(OH)2悬浊液在加热条件下反应得到砖红色沉淀Cu2O.
)可与新制含有NaOH的Cu(OH)2悬浊液在加热条件下反应得到砖红色沉淀Cu2O. 分子中含有σ键的数目为11mol.
分子中含有σ键的数目为11mol. 分子中碳原子轨道的杂化类型是sp2.
分子中碳原子轨道的杂化类型是sp2. +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$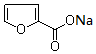 +Cu2O↓+3H2O.
+Cu2O↓+3H2O. 分析 (1)Cu+核外有28个电子,Cu原子失去1个电子生成Cu+,失去的电子数是其最外层电子数,根据构造原理书写Cu+基态核外电子排布式;
(2)单键都为σ键,双键中有1个σ键;
(3)根据价层电子对互斥理论确定原子杂化方式,价层电子对个数=σ键个数+孤电子对个数;
(4)原子个数相等、价电子数相等的微粒互为等电子体,等电子体的结构相似;
(5)以顶点Cu原子为研究对象,与之最近的Cu原子位于面心,每个顶点为8个晶胞共用,据此进行解答;
(6)氢氧化钠溶液中,醛和新制氢氧化铜悬浊液发生氧化还原反应生成羧酸钠、氧化亚铜和水.
解答 解:(1)Cu+核外有28个电子,Cu原子失去1个电子生成Cu+,失去的电子数是其最外层电子数,根据构造原理知Cu+基态核外电子排布式1s22s22p63s23p63d10或[Ar]3d10 ,
故答案为:1s22s22p63s23p63d10或[Ar]3d10 ;
(2)碳为四价,氧为2价,氢为1价,1mol 分子中,含有4molC-H键,2molC-C、2molC-O,1molC=O、2molC=C,所以σ键的数目为11mol,
分子中,含有4molC-H键,2molC-C、2molC-O,1molC=O、2molC=C,所以σ键的数目为11mol,
故答案为:11;
(3) 分子中,每个碳原子含有3个σ 键,和1个π键,且不含孤电子对,所以采取sp2杂化,
分子中,每个碳原子含有3个σ 键,和1个π键,且不含孤电子对,所以采取sp2杂化,
故答案为:sp2;
(4)OH-原子个数为2、价电子数为8,与OH-互为等电子体的一种分子为HF,
故答案为:HF;
(5)以顶点Cu原子为研究对象,与之最近的Cu原子位于面心,每个顶点为8个晶胞共用,铜晶体中每个铜原子周围距离最近的铜原子数目为$\frac{3×8}{2}$=12,
故答案为:12;
(6)氢氧化钠溶液中,糠醛和新制氢氧化铜悬浊液发生氧化还原反应,醛基被氧化成羧基,生成羧酸钠、氧化亚铜和水,反应方程式为NaOH+ +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+3H2O,
+Cu2O↓+3H2O,
故答案为:NaOH+ +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+3H2O.
+Cu2O↓+3H2O.
点评 本题考查了物质结构与性质的有关知识,涉及核外电子排布式的书写、σ键的数目判断、原子杂化方式的判断、等电子体、晶胞结构、醛基的性质等知识点,根据构造原理、价层电子对互斥理论等知识点来分析解答,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
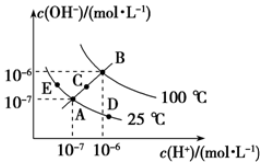 已知水的电离平衡曲线如图所示,
已知水的电离平衡曲线如图所示,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 200g63%的浓硝酸中含氧原子个数为6NA | |
| B. | 50mL12mol•L-1 盐酸和足量MnO2共热,转移的电子数目为0.3NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标况下)气体时,电路中通过的电子数目为4NA | |
| D. | 若CH3COONa溶液中CH3COO-的数目为6NA,则Na+的目为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两者生成硝酸铜的物质的量不同 | |
| B. | 浓硝酸产生的气体更少 | |
| C. | 稀硝酸被还原之后的生成物的价态更低,所以稀硝酸的氧化性更强 | |
| D. | 两个反应中的电子转移的数目相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 侯氏制碱法的工艺过程中主要应用了物质熔沸点的差异 | |
| B. | “熬胆矾铁釜,久之亦化为铜”,该过程发生了分解反应 | |
| C. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于物理变化 | |
| D. | 钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;
;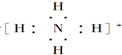 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com