
����Ŀ������ˮ�к�����ᵼ�����ж���ˮ�����ܽ������Ҫ��As( ��)�������κ�As(V)��������ʽ���ڡ�
(1)������Ϊͬһ����Ԫ�أ���ԭ�ӽṹʾ��ͼΪ___________________��
(2)����Ԫ�������ɣ�����˵����ȷ����____________________(����ĸ����)��
a.����������Ӧˮ��������ԣ�S>P>As b. ԭ�Ӱ뾶��S>P>As c.�ǽ����ԣ�S>P>As
(3)���ڵ���ˮ�������Դ�ж��ּ��裬����һ����Ϊ�Ǹ�����Ļ�����(FeS2)������ΪFe(OH)3��ͬʱ����SO42-���������������������ˮ��FeS2��O2���������ӷ���ʽΪ_________________________��
(4)ȥ��ˮ���е��飬���Ƚ�As(�� )ת��ΪAs(V)��ѡ��NaClO��ʵ�ָ�ת����
��֪��Ͷ��ǰˮ��pH=5.81��0.1 mol/L NaClO��ҺpH=10.5����Һ�����������õ������Ǵ����ᡣ
�о�NaClOͶ������As(��)�����ʵ�Ӱ��õ����½����
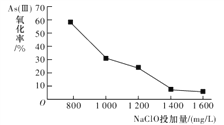
�����˽����ԭ����_________________________��
(5)ǿ�����ӽ�����������������������ʽ���ڵ�As(V)���Ӷ��ﵽȥ��As��Ŀ�ġ�
��֪��һ�������£�As(V)�Ĵ�����ʽ���±���ʾ��
pH | <2 | 2��7 | 7��11 | 11��14 |
������ʽ | H3AsO4 | H2AsO4- | HAsO42- | HAsO42-��AsO43- |
pH=6ʱ��NaClO����������(H3AsO3)�����ӷ���ʽ��_____________________��
���𰸡�  ac 4FeS2+15O2+14H2O=4Fe(OH)3+8SO42-+16H+ ���������õ������Ǵ����ᣬNaClO��Һ�Լ��ԣ���NaClOͶ��������ʱ��NaClO��ҺŨ��������Һ������ǿ��ˮ��̶Ƚ��ͣ�����������ɣ�����As(��)�����ʽ��� HClO+H3AsO3=H2AsO4-+Cl-+2H+
ac 4FeS2+15O2+14H2O=4Fe(OH)3+8SO42-+16H+ ���������õ������Ǵ����ᣬNaClO��Һ�Լ��ԣ���NaClOͶ��������ʱ��NaClO��ҺŨ��������Һ������ǿ��ˮ��̶Ƚ��ͣ�����������ɣ�����As(��)�����ʽ��� HClO+H3AsO3=H2AsO4-+Cl-+2H+
����������1����λ�ڵ������ڵ�VA�壬ԭ������Ϊ15����ԭ�ӽṹʾ��ͼΪ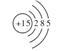 ��
��
��2��ͬ����Ԫ����ԭ������������ԭ�Ӱ뾶��С��Ԫ�طǽ�������ǿ������������Ӧˮ�����������ǿ��ͬ����Ԫ����ԭ������������ԭ�Ӱ뾶����Ԫ�طǽ����Լ���������������Ӧˮ��������Լ�����S��Pͬ���ڣ�ԭ������S>P��P��Asͬ���壬ԭ������As>P����������������Ӧˮ��������ԣ�S>P>As��ԭ�Ӱ뾶��As>P>S���ǽ����ԣ�S>P>As����a��c��ȷ��b����
��3�������⣬FeS2��O2����ΪFe(OH)3��ͬʱ����SO42-������ԭ���غ㣬ˮӦ���뷴Ӧ�������ӷ���ʽΪ��4FeS2+15O2+14H2O=4Fe(OH)3+8SO42-+16H+��
��4����ͼ�ɵã�����NaClOͶ����������As(��)�����ʽ��ͣ������⣬��Һ�����������õ������Ǵ����ᣬ��NaClO��Һ�Լ��ԣ���Ͷ������ʱ����Һ������ǿ��NaClO��ҺŨ������ˮ��̶Ƚ��ͣ�����������ɣ�����As(��)�����ʽ�����
��5������֪��Һ�����������õ������Ǵ�������pH=6ʱ��NaClO��Һ������HClO�����ɱ������ݿɵ�pH=6ʱ��As(V)�Ĵ�����ʽΪH2AsO4-������pH=6ʱNaClO����������(H3AsO3)�����ӷ���ʽ�ǣ�HClO+H3AsO3=H2AsO4-+Cl-+2H+��


 Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д�
Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д� �������Ͽ�ʱͬ��ѵ��ϵ�д�
�������Ͽ�ʱͬ��ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������;�㷺����Ҫ��������Ӳ�ʻ����µĺϽ��Լ����ݵĵ�˿�������£����ܱ���������H2��ԭWO3�ɵõ������٣����ܷ�ӦΪ��
WO3(s) + 3H2(g)![]() W (s) + 3H2O (g)����ش��������⣺
W (s) + 3H2O (g)����ش��������⣺
��1��������Ӧ�Ļ�ѧƽ�ⳣ������ʽΪ____________________��
��2�� ij�¶��·�Ӧ��ƽ��ʱ��H2��ˮ�����������Ϊ2:3����H2��ƽ��ת����Ϊ___________�����¶ȵ����ߣ�H2��ˮ����������ȼ�С����÷�ӦΪ ��Ӧ��������������������������
��3����H2��ԭWO2Ҳ�ɵõ������١���֪��
WO2(s) + 2H2(g)![]() W (s) + 2H2O (g) ��H =" +66.0" kJ��mol�C1
W (s) + 2H2O (g) ��H =" +66.0" kJ��mol�C1
WO2(g) + 2H2(g)![]() W (s) + 2H2O (g) ��H =��137.9 kJ��mol�C1
W (s) + 2H2O (g) ��H =��137.9 kJ��mol�C1
��WO2(s)![]() WO2(g) ����H = ______________________��
WO2(g) ����H = ______________________��
��4����˿�ƹ��е�W��ʹ�ù����л����ӷ���ʹ��˿��ϸ������I2���ӳ��ƹܵ�ʹ���������乤��ԭ��Ϊ��W (s) +2I2(g)![]() WI4(g)������˵����ȷ����________������ţ���
WI4(g)������˵����ȷ����________������ţ���
a���ƹ��ڵ�I2��ѭ��ʹ�� b��WI4�ڵ�˿�Ϸֽ⣬������W�ֳ����ڵ�˿��
c��WI4�ڵƹܱ��Ϸֽ⣬ʹ�ƹܵ������ӳ�
d���¶�����ʱ��WI4�ķֽ����ʼӿ죬W��I2�Ļ������ʼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾ�������µ�������ͨ���������û����ֿ����������������ͬ�����ҳ���һ����NO�����ҳ���һ����O2����ǡ��ʹ�������������ܶ���ͬ��������ʹNO��O2��ַ�Ӧ�һָ������£���Ӧ����:2NO+O2=2NO2��������NO2ת��ΪN2O4�������ж���ȷ����
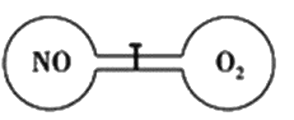
A. ��Ӧǰ�����ҵ�ѹǿ��ͬ
B. ��Ӧ�������ڵ��ܶ��뷴Ӧǰ����ͬ
C. ��ʼʱ���������еķ�������ͬ
D. ��Ӧ����������O2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡ�����ʵ���Ũ�ȵ�NaOH��Һ���ݣ�ÿ��50mL�������зֱ�ͨ��һ������CO2���壬����ȡ��Һ10mL�����ֱ��ˮϡ�͵�100mL���ֱ���ϡ��Һ�����Һ����μ���0.1mol/L�����ᣬ����CO2��������(��״��)�����������������֮��Ĺ�ϵ����ͼ(a)(b)��ʾ���ش��������⣺
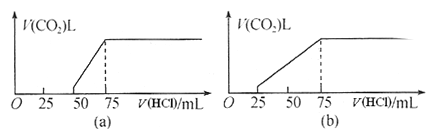
(1)��(a)����£�����Ϊ(д��ѧʽ)___________�������ʵ���֮����__________����״����CO2��������Ϊ________��
(2)��(b)����£�����Ϊ(д��ѧʽ)____________����״����CO2��������Ϊ________��ԭNaOH��Һ�����ʵ���Ũ��Ϊ_________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����е����������Ӧʱ�����ı䷴Ӧ����(�¶ȡ���Ӧ��������)����ѧ��Ӧ�ı��ʲ����ı����( )
A. Na��O2 B. Cu������ C. Na2O2��CO2 D. ľ̿(C)��O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʯ�ͷ���õ��������Ϳ���Pt�������������ת��Ϊ��������������AΪԭ�Ϻϳ����ָ߷��Ӳ��ϵ�·������ͼ��ʾ��

��֪������Ϣ��
��B�ĺ˴Ź���������ֻ��1��壬GΪһ�ȴ�����
�� R-X+R�@-X ![]() R- R�@(X����±��ԭ�ӣ�R��R�@��������)��
R- R�@(X����±��ԭ�ӣ�R��R�@��������)��
��ش��������⣺
(1) B�Ļ�ѧ����Ϊ______________________��
(2)��G����H�Ļ�ѧ����ʽΪ_____________________��
(3) J�Ľṹ��ʽΪ_________________��
(4)��F�ϳɶ����Ļ�ѧ����ʽΪ________________________��
(5)���ͬ���칹������ͬʱ�������������Ĺ���____________��(���������칹)��
�����뱥��NaHCO3��Һ��Ӧ�������壻
�ڼ��ܷ���������Ӧ�����ܷ���ˮ�ⷴӦ��
���к˴Ź�����������4��壬�ҷ����֮��Ϊ6��2��1��1����_________________(д������һ�ֵĽṹ��ʽ)��
(6)���������ϳ�·�ߣ���2-�������һ�ȼ���Ϊԭ��(���Լ���ѡ)������Ʊ�������E�ĺϳ�·��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ���ܴ����������
A. ��ɫ������Һ�У�Fe3+��Mg2+��SCN�C��Cl�C
B.  =1��1012����Һ�У�K+��Na +��CO32����NO3��
=1��1012����Һ�У�K+��Na +��CO32����NO3��
C. c(Fe2+) =1mol��L1����Һ�У�K+��NH4����MnO4����SO42��
D. ��ʹ���ȱ�����Һ�У�Na+��NH4����SO42����HCO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȷ��ʾ���з�Ӧ�����ӷ���ʽ��
A. �ù���ʯ�������չ�ҵβ���е�SO2: Ca2++2OH-+SO2��CaSO3 ��+ H2O
B. ������KMnO4��Һ��H2O2��Ӧ��֤��H2O2���л�ԭ�ԣ�2MnO4��+6H++5H2O2��2Mn2++5O2 ��+8H2O
C. ��ͭ���缫���NaCl��Һ:2C1��+2H2O![]() H2��+Cl2��+2OH-
H2��+Cl2��+2OH-
D. �� Fe2O3���뵽 HI ��Һ�У�Fe2O3+ 6H+��2Fe3+ +3H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڽ���������в���ȷ����
A. ������������������������Һ
B. ��Һ�����塢��Һ�ĸ��������Ƿ�ɢ������ֱ���Ĵ�С
C. ������һ�������»ᷢ���۳�
D. ����������ͨ����Ĥ������ͨ����ֽ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com