
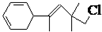
 ,关于该有机物下列叙述正确的是( )
,关于该有机物下列叙述正确的是( )| A、不溶于水 |
| B、属于芳香族化合物 |
| C、在加热和催化剂作用下,最多能和4mol H2反应 |
| D、既能发生氧化反应也能发生加聚反应 |


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
| A、反应容器内的压强不随时间变化 |
| B、P和S的生成速率相等 |
| C、反应混合气体的平均相对分子质量不随时间变化 |
| D、反应混合气体的密度不随时间变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某化学反应2A(g)?B(g),反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )
某化学反应2A(g)?B(g),反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )| A、该反应为放热反应 |
| B、催化剂无法改变该反应的焓变 |
| C、催化剂不能改变反应路径,但能降低该反应的活化能 |
| D、生成物B比反应反应物A更稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH+HCl=NaCl+H2O | ||||
| B、Zn+2HCl=ZnCl2+H2↑ | ||||
C、MnO2+4HCl(浓)
| ||||
| D、CuO+2HCl=CuCl2+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
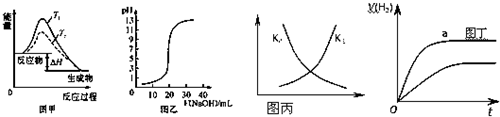
| A、图甲表示温度T1>T2,SO2与O2反应过程中的能量变化 |
| B、图乙表示0.1000mol/L NaOH溶液滴定20.00mL 0.1000mol/L CH3COOH溶液所得到的滴定曲线 |
| C、图丙表示恒容密闭容器中反应“2SO2(g)+O2(g)?2SO3(g)△H<0”的平衡常数K正、K逆随温度的变化 |
| D、图丁表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
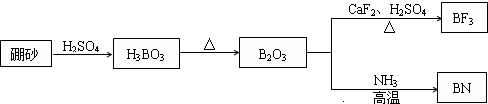
| Na2B2O7 | CaF2 | H3BO3 | NH3 | |
| A | 原子晶体 | 金属晶体 | 原子晶体 | 分子晶体 |
| B | 离子晶体 | 分子晶体 | 离子晶体 | 分子晶体 |
| C | 离子晶体 | 离子晶体 | 分子晶体 | 分子晶体 |
| D | 分子晶体 | 离子晶体 | 分子晶体 | 离子晶体 |

查看答案和解析>>
科目:高中化学 来源: 题型:
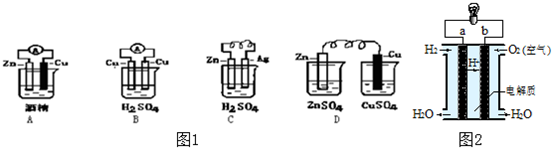
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com