
| A、NaHCO3═Na++H++CO32- |
| B、NaHSO4═Na++H++SO42- |
| C、H2SO4═2H++SO4- |
| D、KClO3═K++Cl-+3O2- |


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
| A、Fe2+、Na+、SO42-、H2O2 |
| B、CH3CHO、MnO4-、H+、K+ |
| C、Pb2+、K+、SO42-、Cl- |
| D、Na+、SO32-、CH3COO-、S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、中子数为20的氯原子:37Cl |
B、Cl-的结构示意图 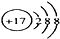 |
C、氢氧根离子的电子式: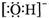 |
| D、HClO的结构式 H-Cl-O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol N2所含有的原子数为NA |
| B、标准状况下,22.4 L水中含有的水分子数为NA |
| C、标准状况下,22.4 L氯化氢所含的原子数为NA |
| D、32 g O2分子和32 g O3分子所含的氧原子数目相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向Al2(SO4)3溶液中加过量的NaOH溶液可制备Al(OH)3 |
| B、将过量的过氧化钠投入FeCl2溶液中,最终看到白色沉淀 |
| C、用稀硫酸清洗做焰色反应的铁丝 |
| D、镁合金的硬度和强度均高于纯镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| HCl |
| X |
| A、NH3?H2O |
| B、CO2 |
| C、NaOH |
| D、HCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com