
【题目】下列表示对应化学反应的离子方程式正确的是( )
A. 用白醋除铁锈:Fe2O3+6H+==3H2O+2Fe3+
B. 向NH4HCO3溶液中加入过量的Ba(OH)2溶液并加热:Ba2++2OH-+NH4++HCO3-![]() NH3↑+2H2O+BaCO3↓
NH3↑+2H2O+BaCO3↓
C. 氯化亚铁溶液在空气中慢慢滴入过量氨水,产生白色沉淀:Fe2++2NH3H2O=Fe(OH)2↓+2NH4+
D. NH4HS溶液与少量的NaOH溶液反应:NH4++OH-=NH3·H2O
【答案】B
【解析】分析:A.醋酸是弱电解质;
B.氢氧化钡过量,碳酸氢铵全部反应;
C.根据氢氧化亚铁易被氧化分析;
D.氢氧化钠不足,HS-首先反应。
详解:A. 醋酸难电离,用白醋除铁锈:Fe2O3+6CH3COOH=3H2O+2Fe3++6CH3COO-,A错误;
B. 向NH4HCO3溶液中加入过量的Ba(OH)2溶液并加热生成碳酸钡、氨气和水:Ba2++2OH-+NH4++HCO3-![]() NH3↑+2H2O+BaCO3↓,B正确;
NH3↑+2H2O+BaCO3↓,B正确;
C. 氯化亚铁溶液在空气中慢慢滴入过量氨水,先产生白色沉淀,然后迅速转化为灰绿色,最后转化为红棕色,C错误;
D. 硫氢根离子结合氢氧根的能力强于铵根,则NH4HS溶液与少量的NaOH溶液反应:HS-+OH-=S2-+H2O,D错误。答案选B。


科目:高中化学 来源: 题型:
【题目】实验室用镁和硝基苯制取反式偶氮苯(溶解性:不溶于水,溶于醇、醚)。实验原理如下:
2![]() +4Mg+8CH3OH→
+4Mg+8CH3OH→ +4Mg(OCH3)2+4H2O
+4Mg(OCH3)2+4H2O
已知:①Mg(OCH3)2在水中极易水解。
②反式偶氮苯产品在紫外线照射后部分转化为顺式偶氮苯。
实验流程如下:

(1)反应中,硝基苯变为反式偶氮苯的反应属于_______________
A、取代反应 B、消去反应 C、还原反应 D、氧化反应
(2)在反应装置中,加入原料及溶剂,搅拌下加热回流。反应加入的镁屑应该_______________________________________。

(3)反应结束后将反应液倒入冰水中,用乙酸中和至中性,即有反式偶氮苯粗产品析出,抽滤(抽滤装置如图1),滤渣用95%乙醇水溶液重结晶提纯。
①为了得到较大颗粒的晶体,加入乙酸时需要____________(填“缓慢加入”、“快速加入”)。
②抽滤过程中要洗涤粗产品,下列液体最合适的是___________。
A.乙醚 B.蒸馏水 C.95%乙醇水溶液 D.饱和NaCl溶液
③抽滤完毕,应先断开橡皮管______________(填序号),以防倒吸。
④重结晶操作包括“加热溶解、趁热过滤、冷却结晶、抽滤、洗涤、干燥”。上述重结晶过程中的________________________操作除去了可溶性杂质。
(4)已知薄层色谱分析中,分子极性弱的物质,在溶剂中扩散更快。某同学采用薄层色谱分析所得偶氮苯,实验开始时和展开后的斑点如图2所示。展开后的斑点中,顺式偶氮苯为______(填斑点序号),说明顺式偶氮苯的分子极性比反式偶氮苯的分子极性__________(填“强”或“弱”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙酸铜是合成优良催化剂、传感材料﹣﹣纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:
![]() ;
;![]()
制备苯乙酸的装置示意图如图(加热和夹持装置等略):
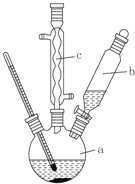
已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇。回答下列问题:
(1)在250mL三口瓶a中加入70mL 70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是______。
(2)将a中的溶液加热至100℃,缓缓滴加40g苯乙腈到硫酸溶液中,然后升温到130℃继续反应。在装置中,仪器b的作用是滴加苯乙腈;仪器c的作用是__________。反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是_________。下列仪器中可用于分离苯乙酸粗品的是_________(填标号)。
A.分液漏斗 B.漏斗 C.烧杯 D.直形冷凝管 E.玻璃棒
(3)提纯粗苯乙酸的方法是_________,最终得到44g纯品,则苯乙酸的产率是__________。(小数点后保留一位)(相对分子质量:苯乙腈117;苯乙酸136)
(4)用CuCl22H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是___________。
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱溶液中都含有OH-,因此不同的碱表现出一些共同的性质。下列关于Ba(OH)2性质的描述中不属于碱的共同性质的是( )
A.能使紫色石蕊试液变蓝色B.能与盐酸反应生成水
C.能与Na2S04溶液反应生成BaS04沉淀D.能与CO2反应生成水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年10月,屠呦呦因发现青蒿素和双氢青蒿素治疗疟疾的新疗法而获得诺贝尔生理学或医学奖。双氢青蒿素的化学式为C15H24O5,相对分子质量为284。下面关于双氢青蒿素的说法正确的是( )
A. 1 mol双氢青蒿素的质量为284 g· mol-1
B. 双氢青蒿素的摩尔质量等于它的相对分子质量
C. 14.2 g双氢青蒿素中含有的原子总数为2.2NA
D. 含有6.02×1023个碳原子的双氢青蒿素的物质的量为1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素A、B、C、D 原子序数依次增大且最外层电子数之和为17。B、D 同主族,短周期中C原子半径最大,B最外层电子数是次外层的3倍。下列推断不正确的是
A. 元素B、C、D 形成的化合物的水溶液呈中性
B. 元素B、C 形成的化合物中可能既含有离子键又含共价键
C. 离子半径从大到小的顺序为D>B>C
D. 元素B 的简单气态氢化物的热稳定性比D 的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.(1)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①假设用酸性高锰酸钾溶液吸收煤燃烧产生的SO2,该过程中高锰酸根被还原为Mn2+,请写出该过程的离子方程式______________。
②将燃煤产生的二氧化碳加以回收,可降低碳的排放。左图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图,a电极名称:_____________(填“正极”或“负极”),b电极的反应式:________________________。

(2)如果采用NaClO、Ca(ClO)2作吸收剂,也能得到较好的烟气脱硫效果。
已知下列反应:
SO2(g)+2OH-(aq) ==SO32-(aq)+H2O(l) ΔH1
ClO-(aq)+SO32-(aq) ==SO42-(aq)+Cl-(aq) ΔH2
CaSO4(s)==Ca2+(aq)+SO42-(aq) ΔH3
则反应SO2(g)+ Ca2+(aq)+ ClO-(aq) +2OH-(aq) = CaSO4(s) +H2O(l) +Cl-(aq)的ΔH=_____。
II.(3)FeO42-在水溶液中的存在形态如图所示。

①若向pH=10的这种溶液中加硫酸至pH=2,HFeO4-的分布分数的变化情况是__________。
②若向pH=6的这种溶液中滴加KOH溶液,则溶液中含铁元素的微粒中,_________转化为_________(填微粒符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验发现,298 K时,在FeCl3酸性溶液中加少量锌粒后,Fe3+立即被还原成Fe2+。某夏令营兴趣小组根据该实验事实设计了如图所示原电池装置。下列有关说法正确的是( )
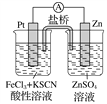
A. 该原电池的正极反应是Zn-2e-===Zn2+
B. 左烧杯中溶液的血红色逐渐褪去
C. 该电池铂电极上有气泡出现
D. 该电池总反应为3Zn+2Fe3+===2Fe+3Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示,下列说法正确的是

A. 电子从b流出,经外电路流向a
B. HS-在硫氧化菌作用下转化为SO42-的反应是HS-+4H2O-8e-=SO42-+9H+
C. 如果将反应物直接燃烧,能量的利用率不会变化
D. 若该电池电路中有0.4mol电子发生转移,则有0.5molH+通过质子交换膜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com