
【化学与技术】
将磷肥生产中形成的副产物石膏(CaSO4·2H2O)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。以下是石膏转化为硫酸钾和氯化钙的工艺流程示意图。

(1)本工艺中所用的原料除CaSO4·2H2O、KCl外,还需要 等原料。
(2)石膏悬浊液中加入碳酸铵溶液后发生反应的离子方程式为 。
(3)过滤Ⅰ操作所得固体中,除CaCO3外还含有 (填化学式)等物质,该固体可用作生产水泥的原料。
(4)检验过滤Ⅰ所得滤液中含有CO32-的方法是 。
(5)氯化钙结晶水合物(CaCl2·6H2O)是目前常用的无机储热材料,选择的依据是 。
a.熔点较低(29℃熔化) b.能导电 c.能制冷 d.无毒
(6)上述工艺流程中体现绿色化学理念的是 。
(1)CaCO3、NH3、H2O
(2)CaSO4+CO32-=CaCO3+SO42-
(3)CaSO4
(4)滤液中滴加盐酸产生气泡
(5)ad
(6)碳酸钙用于制取水泥原料、硫酸钙和氯化钾转化为硫酸钾和氯化钙、氨在工艺中循环使用等(原子利用率高,没有有害物质排放到环境中)
【解析】(1)根据流程可知,需要生石灰、二氧化碳、氨气、水、碳酸钙高温分解即生成氧化钙和二氧化碳,所以本工艺中所用的原料除CaSO4·2H2O、KCl外,还需要CaCO3、NH3、H2O等原料。
(2)碳酸钙的溶解度小于硫酸钙,因此根据沉淀转化原理知,石膏悬浊液中加入碳酸铵溶液后发生的离子方程式为CaSO4+CO32-=CaCO3+SO42-。
(3)硫酸钙微溶于水,所以过滤I操作所得固体中,除CaCO3外还含有CaSO4等物质。
(4)由于碳酸盐能和盐酸反应产生二氧化碳气体,所以检验过滤I所得滤液中含有CO32-的方法是滤液中滴加盐酸产生的气泡。
(5)储热材料与物质的导电性以及能否制冷无关系,而与自身的熔点高低和有无毒性无关系,所以选ad。
(6)根据流程图知,工艺流程中体现绿色化学理念的是反应中产生的碳酸钙用于制取水泥原料、硫酸钙和氯化钾转化为硫酸钾和氯化钙、氨在工艺中循环使用等。


科目:高中化学 来源:2014高考名师推荐化学NA与粒子(解析版) 题型:选择题
用NA表示阿伏伽德罗常数的值。下列叙述中不正确的是
A.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA
B.28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
C.常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
D.常温常压下,22.4L氯气于足量的镁粉反应,转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测8 题型:选择题
下列关于有机物的叙述不正确的是
A.甲烷、甲苯、乙醇、乙酸都可以发生取代反应
B.煤中含有苯、甲苯、二甲苯等芳香烃,可通过干馏制取
C.乙酸乙酯在无机酸或碱存在时都能发生水解反应
D.淀粉、纤维素、蛋白质都属于高分子化合物
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测7 题型:选择题
肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知:
N2(g)+2O2(g)=2NO2(g) ΔH=+67.7kJ/mol,
2N2H4(g)+2NO2(g)=3N2(g) +4H2O(g) ΔH=-1135.7kJ/mol,
下列说法正确的是
A.N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-1068 kJ/mol
B.肼是与氨类似的弱碱,它易溶于水,其电离方程式:N2H4 + H2O=N2H5++ OH-
C.铂做电极,以KOH溶液为电解质溶液的肼—空气燃料电池,放电时的负极反应式:N2H4-4e-+4OH-=N2↑+4H2O
D.铂做电极,以KOH溶液为电解质溶液的肼—空气燃料电池,工作一段时间后,KOH溶液的pH将增大
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测6 题型:选择题
某离子反应中涉及H2O、ClO—、NH4+、H+、N2、Cl—六种微粒。其中N2的物质的量随时间变化的曲线如右图所示。下列判断正确的是:
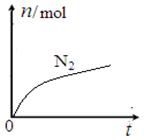
A该反应的还原剂是Cl—
B消耗1 mol还原剂,转移6 mol电子
C氧化剂与还原剂的物质的量之比为2:3
D反应后溶液的酸性明显增强
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测6 题型:选择题
在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t℃时AgCl的Ksp=4×10-10。下列说法不正确的是
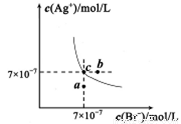
A.在t℃时,AgBr的Ksp为4.9×10-13
B.在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点
C.图中a点对应的是AgBr的不饱和溶液
D.在t℃时,AgCl(s)+Br-(aq)  AgBr(s)+Cl-(aq)平衡常数K≈816
AgBr(s)+Cl-(aq)平衡常数K≈816
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测5 题型:选择题
下列表达不正确的是
A.NaHS在水中的电离方程式为:NaHS=Na++HS- 和HS-  H++S2-
H++S2-
B.同物质的量浓度的氨水和盐酸反应至中性时所用体积:V(NH3·H2O)<V(HCl)
C.Na2SO3溶液中:c(H+)+ c(HSO3-)+ 2c(H2SO3)= c(OH-)
D.同浓度的下列溶液中,c (CH3COO-)的大小:CH3COONa>CH3COONH4>CH3COOH
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测3 题型:选择题
短周期元素R、T、Q、W、G在元素周期表中的相对位置如下图所示,其中Q是无机非金属材料的主角。下列判断正确的是
|
| R |
| |
T | Q |
| W | G |
A.离子半径:T< W< G
B.最简单气态氢化物的热稳定性:
C.最高价氧化物对应水化物的酸性:Q >W>G
D.T和G组成的化合物甲溶于水,其水溶液呈中性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com