
 与足量浓溴水反应的化学方程
与足量浓溴水反应的化学方程
| ||
| ||
| ||
| ||
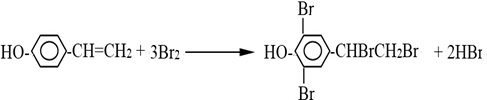 ,故答案为:
,故答案为: ;
;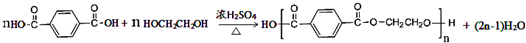 ,故答案为:
,故答案为: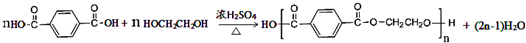 .
.


科目:高中化学 来源: 题型:
| A、锡 | B、碲 | C、锑 | D、镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只含一个双键的直链有机物 |
| B、含两个双键的直链有机物 |
| C、只含一个环的环状有机物 |
| D、只含一个双键的环状有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 和
和 的物质互为同分异构体,我们称之为顺反异构.则分子式为C5H10的有机物,属于烯烃的同分异构体的数目为
的物质互为同分异构体,我们称之为顺反异构.则分子式为C5H10的有机物,属于烯烃的同分异构体的数目为 的二氯代物有
的二氯代物有 的二氯代物有
的二氯代物有查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
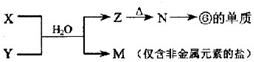
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
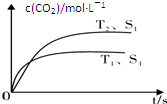
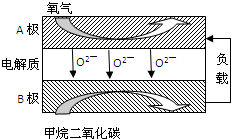
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、植物油不能发生水解反应 |
| B、淀粉水解的最终产物是麦芽糖 |
| C、油脂在人体内水解产生高级脂肪酸和甘油 |
| D、蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com