
 反应N2O4(g)?2NO2(g);△H=+57kJ•mol-l,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法不正确的是( )
反应N2O4(g)?2NO2(g);△H=+57kJ•mol-l,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法不正确的是( )| A. | A、C两点气体的平均相对分子质量:A>C | |
| B. | A、C两点气体的颜色:A深,C浅 | |
| C. | 由状态B到状态A,可以用加热的方法 | |
| D. | A、C两点的反应速率:A<C |
分析 N2O4(g)═2NO2(g)△H=+57kJ•mol-1,该反应为吸热反应,升高温度,化学平衡正向移动,NO2的体积分数增大;增大压强,化学平衡逆向移动,NO2的体积分数减小,结合图象来分析解答.
A、增大压强,化学平衡逆向移动,C点时气体的物质的量小,混合气体的总质量不变,据此判断;
B、增大压强平衡向逆反应进行,向逆反应进行是减小由于压强增大导致浓度增大趋势,但到达平衡仍比原平衡浓度大;
C、压强相同,升高温度,化学平衡正向移动,NO2的体积分数增大,A点NO2的体积分数大;
D、A、C两点都在等温线上,压强越大,反应速率越快.
解答 解:A.由图象可知,A、C两点都在等温线上,C的压强大,增大压强,化学平衡逆向移动,C点时气体的物质的量小,混合气体的总质量不变,则平均相对分子质量大,即平均相对分子质量:A<C,故A错误;
B.由图象可知,A、C两点都在等温线上,C的压强大,与A相比C点平衡向逆反应进行,向逆反应进行是由于减小体积增大压强,平衡移动的结果降低NO2浓度增大趋势,但到达平衡仍比原平衡浓度大,平衡时NO2浓度比A的浓度高,NO2为红棕色气体,则A、C两点气体的颜色:A浅,C深,故B错误;
C.升高温度,化学平衡正向移动,NO2的体积分数增大,由图象可知,A点NO2的体积分数大,则T1<T2,由状态B到状态A,可以用加热的方法,故C正确;
D.由图象可知,A、C两点都在等温线上,C的压强大,则A、C两点的反应速率:A<C,故D正确;
故选:AB.
点评 本题考查化学平衡的图象,明确外界条件对化学平衡的影响及图象中纵横坐标的含义、“定一议二”“先拐先平”原则即可解答,难度不大.注意B选项为易错点,改变压强的本质为体积变化.


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 160与180互为同位素;H${\;}_{2}^{16}$O、D${\;}_{2}^{18}$O、D${\;}_{2}^{18}$0互为同素异形体 | |
| B. | SiH4、PH3、HCl的稳定性逐渐增强 | |
| C. | 乙烯的结构简式为CH2CH2 | |
| D. | Ca2+的结构示意图为 NH4Cl的电子式为 NH4Cl的电子式为 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 | |
| B. | 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 | |
| C. | 用过滤的方法除去蔗糖溶液中含有的少量淀粉胶体 | |
| D. | 用加热、过滤、蒸发的方法可以除去粗盐中的泥沙、CaCl2、MgCl2等杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2 | B. | CO2 | C. | NO | D. | NO和CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 电离能kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
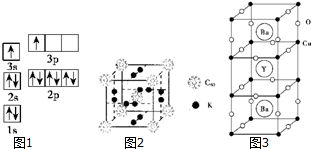
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨基酸和蛋白质都是两性分子;在碱性条件下,氨基酸以阴离子形态存在 | |
| B. | 固体氨基酸主要以内盐形式存在;可以通过控制溶液的pH分离氨基酸 | |
| C. | 强紫外线灼伤人体皮肤属于皮肤蛋白质的变性 | |
| D. | 蛋白质溶液中分别加入浓HNO3、10%NaOH溶液、0.1%茚三酮溶液均产生白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 以下各单质和化合物之间存在如图所示转化关系:
以下各单质和化合物之间存在如图所示转化关系:查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该过程中硫酸是催化剂 | B. | 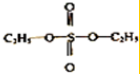 可属于二元酯 可属于二元酯 | ||
| C. | 该过程中①、②是加成反应 | D. | 该过程中③、④是水解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com