
�о�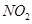 ��
��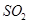 ��CO�ȴ�����Ⱦ����IJ���������������Ҫ���塣
��CO�ȴ�����Ⱦ����IJ���������������Ҫ���塣
��1�� ��ʹ
��ʹ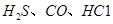 �������������ڶ����ⶨCO�ĺ�������֪��
�������������ڶ����ⶨCO�ĺ�������֪��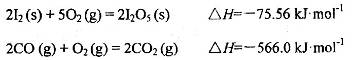
д��CO��g����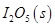 ��Ӧ����
��Ӧ����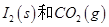 ���Ȼ�ѧ����ʽ��________________��
���Ȼ�ѧ����ʽ��________________��
��2��CO������ȼ�ϵ�أ���KOH��Һ������ʣ��������ֱ����CO�Ϳ��������������У�K+����_______��(���������)��������Ӧ����ʽΪ��___________________��
��3�����Ͱ��������������Ļ�ѧԭ���Dz��ð�ˮ���������е�SO2������һ��������
�����������ղ��ﷴӦ���ü������ŵ�����ܻ�������SO2�⣬���ܵõ�һ�ָ��Ϸ��ϡ�
�ٸø��Ϸ��Ͽ��ܵĻ�ѧʽΪ___________(д��һ�ּ���)��
������ˮ��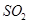 ǡ����ȫ��Ӧ�������Σ����ʱ��Һ��________��(��ᡱ�)��
ǡ����ȫ��Ӧ�������Σ����ʱ��Һ��________��(��ᡱ�)��
������������ʵĵ���ƽ�ⳣ�����£���ˮ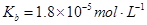

���������Һ��ͨ��________�����ʹ��Һ�����ԡ�(�SO2����NH3��)
��ʱ��Һ�� ________2�������������������
________2�������������������
��4��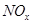 ����ǿ����Һ�����������Ρ������������£�FeSO4��Һ�ܽ�
����ǿ����Һ�����������Ρ������������£�FeSO4��Һ�ܽ�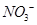 ��ԭΪNO��д���ù����в���NO��Ӧ�����ӷ���ʽ___________________________________��
��ԭΪNO��д���ù����в���NO��Ӧ�����ӷ���ʽ___________________________________��
��ÿ��2�֣�
��1��5CO(g) + I2O5(s) = 5CO2 + I2(s) ?H= -1377.22kJ?mol?1
��2������O2 + 2H2O +4e? = 4OH?
��3���� (NH4)3PO4��(NH4)2HPO4��NH4H2PO4
�ڼ� �� SO2 >
��4��3Fe2+ + NO3? + 4H+ =3Fe3+ +NO��+ 2H2O
���������������1����д����ѧ����ʽ�����������ʵ�״̬��Ȼ����ݸ�˹��������?H��
?H= �� ?H1 +
?H1 +  ?H2������������ݿɵô𰸡�
?H2������������ݿɵô𰸡�
��2��ԭ��ص������Һ�У����������������������ΪKOH��Һ������������ӦΪO2��H2O���������µõ�������OH?��
��3���ٷ�����Ӧ���������������Ӧ���������ᷴӦ�������������ͬ������(NH4)3PO4��(NH4)2HPO4��NH4H2PO4��
�ڰ�ˮ��SO2ǡ����ȫ��Ӧ����(NH4)2SO3��ˮ���Լ��ԡ�
����Ϊ������Һ�Լ��ԣ�����ͨ��SO2���к�OH?��ʹ��Һ�����ԣ����ݵ���غ��֪��[NH4+]+[H+]=[OH?]+2[SO32?]+[HSO3?]����Һ����[H+]=[OH?],��[NH4+]=2[SO32?]+[HSO3?]������[NH4+]/[SO32?]>2��
��4��������Ϣ�ҳ���Ӧ����������ƽ�ɵ����ӷ���ʽ��
���㣺���⿼���Ȼ�ѧ����ʽ����д��ԭ���ԭ���������ˮ�⡢����Ũ�ȱȽϺ����ӷ���ʽ����д��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��1������Һ��ʯ��������Ҫ�ɷ�֮һ�Ƕ���(C4H10)����10 kg������ȫȼ�ղ����ɶ�����̼�����Һ̬ˮʱ���ų�������Ϊ5��105 kJ����д������ȼ�յ��Ȼ�ѧ����ʽ�� ����֪1molҺ̬ˮ����ʱ��Ҫ����44 kJ��������ӦC4H10(g)+6.5O2(g)=4CO2(g)+5H2O(g)�Ħ�H= ��
��2����ͬѧ�ö��������Ϊԭ������һȼ�յ�أ�ͨ�붡���һ��Ϊ ��������ϡ����Ϊ�������Һʱ����������ӦʽΪ ��
��3����֪:Fe(s) +1/2O2(g)=FeO(s) ��H=��272.0kJ��mol-1
2Al(s)+3/2O2(g)=Al2O3(s) ��H=��1675.7kJ��mol-1
Al��FeO�������ȷ�Ӧ���Ȼ�ѧ����ʽ�� ��
��4����֪��1 mol H��H����1 molN��H����1 molN��N���ֱ���Ҫ��������akJ��bkJ��ckJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
����β���ѳ�Ϊ��Ҫ�Ŀ�����Ⱦ�
��1��������ȼ������ʱ����Ӧ��N2(g)+O2(g)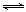 2NO(g)���ǵ�������β���к���NO��ԭ��֮һ��T ��ʱ����5L�ܱ������г���8mol N2��9molO2��5min���ƽ��ʱNO���ʵ���Ϊ6mol������������µ�ƽ�ⳣ����д��������̣���
2NO(g)���ǵ�������β���к���NO��ԭ��֮һ��T ��ʱ����5L�ܱ������г���8mol N2��9molO2��5min���ƽ��ʱNO���ʵ���Ϊ6mol������������µ�ƽ�ⳣ����д��������̣���
��2��H2��CO���Դ���ԭNO�Դﵽ������Ⱦ��Ŀ�ģ�
����֪��N2(g)+ O2(g) = 2NO(g) ��H = +180.5kJ/mol
2H2(g)+ O2(g) = 2H2O(l) ��H = -571.6kJ/mol
��H2(g)��NO(g)��Ӧ����N2(g)��H2O(l)���Ȼ�ѧ����ʽΪ ��
�ڵ�����һ��ʱ�������������ı���������ѧ��Ӧ���ʡ���ͼ�Ƿ�Ӧ��2NO(g) + 2CO(g) 2CO2(g)+ N2(g) ��NO��Ũ�����¶�(T)�����������(S)��ʱ��(t)�ı仯���ߣ��ݴ��жϸ÷�Ӧ�ġ�H 0 (�����������������ȷ����)���������ı����S1��S2 ����ͼ�л���NO��Ũ����T1��S2 �����´ﵽƽ������еı仯���ߣ���ע��������
2CO2(g)+ N2(g) ��NO��Ũ�����¶�(T)�����������(S)��ʱ��(t)�ı仯���ߣ��ݴ��жϸ÷�Ӧ�ġ�H 0 (�����������������ȷ����)���������ı����S1��S2 ����ͼ�л���NO��Ũ����T1��S2 �����´ﵽƽ������еı仯���ߣ���ע��������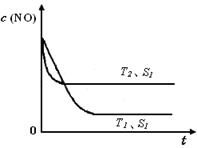
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(Iij���ʳ�������ˮ�еĵ�Ԫ�ض���NH4+��NH3��H2O����ʽ���ڡ������������£�NH4+����������Ӧ��������NO3-��������Ӧ�������仯ʾ��ͼ����: 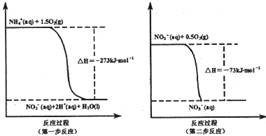
��1��1 mo1NH4+(aq)ȫ��������NO3-(aq)���Ȼ�ѧ����ʽ�� _ ��
��2����һ�������£����ˮ�м���CH3OH����HNO3��ԭ�� N2�����÷�Ӧ����32gCH3OHת��6mol���ӣ���μӷ�Ӧ�Ļ�ԭ���������������ʵ���֮����_ ��
(B)�����ٷɻ���ƽ�������ʱ��β���е�NO���ƻ������㡣��ѧ�������о����ô�����
��β���е�NO��COת���CO2��N2����ѧ����ʽ����:2NOʮ2CO 2CO2+ N2 ��H
2CO2+ N2 ��H
ij�¶��������崫������ò�ͬ��ʱ���NO��COŨ�����±�: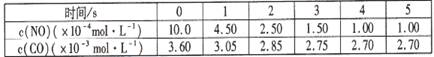
��ش���������(���������¶ȱ仯�Դ�����Ч�ʵ�Ӱ��):
��1�������������·�Ӧ�ܹ��Է����У���Ӧ�ġ�H 0(��д��>������<������=��)
��2���ڸ��¶��£���Ӧ��ƽ�ⳣ��K= (ֻд��������);
��3��ijͬѧ���������ʵ�飬�ֱ���֤�¶ȡ������ȱ�����Ի�ѧ��Ӧ���ʵ�Ӱ����ɣ�
����ʵ���������±�:
��ͬѧ�����˱�������ʵ�������£����������NOŨ����ʱ��仯����������ͼ������ͼ�ϱ����������ߵ�ʵ����; 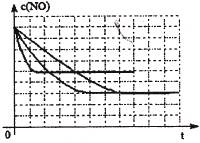
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�������γɶ��ֻ������NH3��N2H4��HCN��NH4NO3�ȡ�
��1����֪��N2(g)+2H2(g)=N2H4(l) ��H=" +" 50.6kJ��mol-1
2H2(g)+O2(g)=2H2O(l) ��H="-571.6" kJ��mol-1
���N2H4(l)+O2(g)=N2(g)+2H2O(l) ��H= kJ��mol-1
��N2(g)+2H2(g)=N2H4(l) �����Է����е�ԭ���� ��
���ô������������������Եõ�N2H4��ϡ��Һ���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��2���ɿ��Һ�е�CN-����H2O2��������֪��H2SO4=H++ HSO4- HSO4-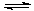 H++ SO42-
H++ SO42-
�ò��缫������������Һ��������������S2O82-��S2O82-ˮ����Եõ�H2O2��д�������ϵĵ缫��Ӧʽ ��
��3������þ������NH4+�ķ�ˮ�ᷢ�����·�Ӧ��
MgO+H2O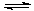 Mg(OH)2 Mg(OH)2+2NH4+
Mg(OH)2 Mg(OH)2+2NH4+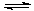 Mg2+ +2NH3��H2O��
Mg2+ +2NH3��H2O��
���¶ȶԵ������ʵ�Ӱ����ͼ��ʾ����25��ǰ�������¶ȵ�ȥ���������ԭ���� ��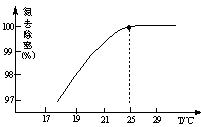
��ʣ�������þ������Է�ˮ�γɶ�����Ⱦ�������� ��
��4���ζ������ˮ�еİ������������������백�������ʽ������ˮ�У��������£���ȡ10 mL��ˮˮ����������ƿ�У��ټ�����ˮ�������Ϊ175 mL���Ƚ�ˮ���������ԣ��ټ�������þʹˮ�������ԣ����Ȣ���25 mL��������������İ�[2NH3+4H3BO3��(NH4)2B4O7+5H2O]�ܽ�����Һ������ƿ�У�����2��ָʾ������c mol��L-1������ζ����յ�[(NH4)2B4O7+H2SO4+5H2O��(NH4)2SO4+4H3BO3]����¼���ĵ����V mL����ˮ���е��ĺ����� mg��L-1���ú�c��V�ı���ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ҵ̼���ƣ�����ԼΪ98�����к���Ca2+��Mg2+��Fe3+��Cl����SO42�������ʣ��ᴿ������·��ͼ��ʾ��
��̼���Ƶı�����Һ�ڲ�ͬ�¶���������������ͼ��ʾ��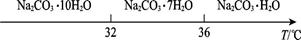
���й����ʵ��ܶȻ�����
| ���� | CaCO3 | MgCO3 | Ca��0H��2 | Mg��OH��2 | Fe��OH��3 |
| Ksp | 4.96��10��9 | 6.82��10��6 | 4.68��10��6 | 5.61��10��12 | 2.64��10��39 |
 Na2CO3��s��+10H2O��g��
Na2CO3��s��+10H2O��g�� ="+532.36" kJ��mol��1
="+532.36" kJ��mol��1 Na2CO3��H2O��s��+9H2O��g��
Na2CO3��H2O��s��+9H2O��g��  ="+473.63" kJ��mol��1
="+473.63" kJ��mol��1�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
��1��NO2����ˮ���գ�Ҳ����NH3������Ҳ����CH4����ԭNOx�������������������Ⱦ�����磺
CH4(g)��4NO2(g)��4NO(g)��CO2(g)��2H2O(g) ��H����574 kJ��mol��1
CH4(g)��4NO(g)��2N2(g)��CO2(g)��2H2O(g) ��H����1160 kJ��mol��1
���ñ�״����2��24L CH4��ԭNO2��N2����������ת�Ƶĵ�������Ϊ______�������ӵ�������ֵ��NA��ʾ�����ų�������Ϊ______kJ��
��2����֪��2SO2(g)+O2(g) 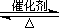 2SO3(g) ?H=-196��6 kJ��mol-1
2SO3(g) ?H=-196��6 kJ��mol-1
2NO(g)+O2(g) 2NO2(g) ?H=-113��0 kJ��mol-1
2NO2(g) ?H=-113��0 kJ��mol-1
��������ӦNO2(g)+SO2 (g) SO3(g)+NO(g)��?H= kJ��mol-1��
SO3(g)+NO(g)��?H= kJ��mol-1��
������һ�������£���NO2��SO2�������1:2�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬���� ��
A��ÿ����1 mol SO3��ͬʱ����1 mol NO2 B����ϵѹǿ���ֲ���
C�����������ɫ���ֲ��� D�� SO3��NO������ȱ��ֲ���
������ij�¶��£�SO2��ƽ��ת����(��)����ϵ��ѹǿ(p)�Ĺ�ϵ����ͼ������ʾ��
ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ��K(A)_______K(B)���������������������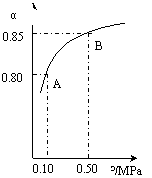
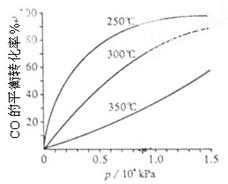
��3��CO�����ںϳɼ״�����Ӧ����ʽΪCO(g)+2H2(g) CH3OH(g)��CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ����ͼ���ң���ʾ���÷�Ӧ?H 0���>���� <������
CH3OH(g)��CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ����ͼ���ң���ʾ���÷�Ӧ?H 0���>���� <������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��20����30�����Eyring��Pzer����ײ���۵Ļ����������ѧ��Ӧ�Ĺ���̬���ۣ���ѧ��Ӧ������ͨ������ײ������ɵģ������ڷ�Ӧ�ﵽ������Ĺ����о���һ���������Ĺ���̬����ͼ����ʾ��NO2��CO��Ӧ����CO2��NO�����е������仯ʾ��ͼ��˵�������Ӧ�� ������ȡ����ȡ�����Ӧ��NO2��CO�������� ���������������������CO2��NO����������

��ij�¶�ʱ����һ��2 L���ܱ������У�X��Y��Z�����������ʵ�����ʱ��ı仯������ͼ����ʾ������ͼ�����ݣ�����д���пհף�
�ٸ÷�Ӧ�� minʱ�ﵽƽ��״̬����Ӧ�ȣ���
�ڸ÷�Ӧ�Ļ�ѧ����ʽΪ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��Դ��ȱ���������ٵ��ش����⡣�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������˼״�����Ϊ21���͵�����ȼ�ϡ�
��1����֪�ڳ��³�ѹ�£�
��2CH3OH(l)+3O2(g) 2CO2(g)+4H2O(g) ��H= ��1275.6 kJ��mol��1
��H2O(l) H2O(g) ��H="+" 44.0 kJ.mo��1
д����ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽ ��
��2����ҵ����CO����ȼ�ϼ״���һ�������·�����Ӧ��CO(g)+2H2(g) CH3OH(g)��ͼ1��ʾ��Ӧ�������ı仯��ͼ2��ʾһ���¶��£������Ϊ2L���ܱ������м���4mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯ͼ��
CH3OH(g)��ͼ1��ʾ��Ӧ�������ı仯��ͼ2��ʾһ���¶��£������Ϊ2L���ܱ������м���4mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯ͼ��
���ڡ�ͼ1���У����� ���a����b������ʾʹ���˴�����
�����жϸ÷�Ӧ�ڡ�ͼ2�������������Ƿ��Ѵﻯѧƽ��״̬�������� ����˫ѡ��
| A��������ѹǿ���� | B����ϵ���ܶȲ���ʱ��ı� |
| C��v��(H2)=2v��(CH3OH) | D��CO��H2�����ʵ����ıȲ���ʱ��ı� |
 CH3OH(g)�Ļ�ѧƽ�ⳣ��K= ��
CH3OH(g)�Ļ�ѧƽ�ⳣ��K= ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com