
【题目】一定温度下,可逆反应A2(g)+3B2(g)![]() 2AB3(g)达到平衡的标志是( )
2AB3(g)达到平衡的标志是( )
A.容器内每减少1mol A2,同时生成2mol AB3
B.容器内每减少1mol A2,同时生成3mol B2
C.容器内A2、B2、AB3的物质的量之比为1:3:2
D.容器内A2、B2、AB3的物质的量浓度之比为1:1:1
【答案】B
【解析】
达到化学平衡状态,正逆反应速率相等,各组分的浓度不变,
A、容器内每减少1mol A2,同时生成2mol AB3,二者均表示的是正反应速率,反应向右进行,该反应没有达到平衡状态,故A错误;
B、容器内每减少1mol A2等效于消耗3mol B2,同时生成3mol B2,正逆反应速率相等,达平衡状态,故B正确;
C、容器内A2、B2、AB3的物质的量之比为1:3:2,物质的量之比无法判断各组分的物质的量是否不变,无法证明正逆反应速率相等,故C错误;
D、容器内A2、B2、AB3的物质的量浓度之比为1:1:1,各组分的浓度之比无法判断浓度是否不变,无法判断是否达到平衡状态,故D错误;
故选:B。


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
【题目】有机化合物M 是合成某种抗新冠肺炎药物的中间体。M 的结构简式如图所示 。下列有关M 的的叙述正确的是
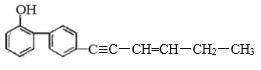
A.该有机物的分子式为 C18H15O
B.lmolM 最多能与 5molBr2 (四氯化碳溶液)发生反应
C.M 分子中至少有11 个碳原子共平面
D.M 分子中至少有5个碳原子在一条直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25 ℃、101 kPa时,1 mol H2与溴蒸气完全反应生成气态溴化氢放出能量Q kJ,则下列热化学方程式书写正确的是 ( )。
A.H2(g)+Br2(g)=2HBr(g) ΔH=-2Q kJ·mol-1
B.H2(g)+Br2(l)=2HBr(g) ΔH=-Q kJ·mol-1
C.![]() H2(g)+
H2(g)+![]() Br2(g)=HBr(g)ΔH=+
Br2(g)=HBr(g)ΔH=+![]() kJ·mol-1
kJ·mol-1
D.HBr(g)=![]() H2(g)+
H2(g)+![]() Br2(g)ΔH=+
Br2(g)ΔH=+![]() kJ·mol-1
kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是恒温下某化学反应的反应速率随反应时间变化的示意图。下列叙述与示意图不相符合的是( )
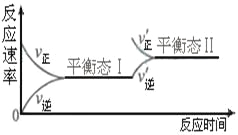
A. 反应达平衡时,正反应速率和逆反应速率相等
B. 该反应达到平衡态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡态Ⅱ
C. 该反应达到平衡态后,减小反应物浓度,平衡发生移动,达到平衡态Ⅱ
D. 同一种反应物在平衡态Ⅰ和平衡Ⅱ时浓度不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W有如图所示的转化关系:

(1)若X单质的一种同素异形体是一种黑色的非金属单质,则Y转化为Z的化学方程式_________________,Z的晶体类型______________晶体。
(2)若X为一种金属的氯化物,Y是一种常见的两性氢氧化物,W为化工常用的强碱,写出Y与W反应的离子方程式_______________________。
(3)若X是一种活泼的金属单质,Z是一种淡黄色的化合物,Z的化学式___________,则Z转化为W的化学方程式________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是部分短周期元素的常见化合价与原子序数的关系图:
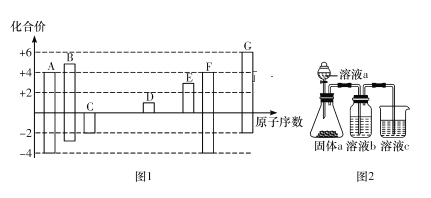
请回答下列问题:
(1)元素F在周期表中的位置为________________
(2)C、D、E、G的简单离子半径由大到小的顺序为_______________(用离子符号表示)。
(3)二元化合物X是含有元素A的18电子分子,3 g X(g)在25 ℃ 101 kPa 下完全燃烧生成稳定的化合物时放出Q kJ的热量,写出表示X燃烧热的热化学方程式:________________
(4)某同学设计实验用图2所示装置证明元素A、B、F的非金属性强弱(其中溶液b和溶液c均足量)。
①溶液b为_________________
②溶液c中发生反应的离子方程式为__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将1.0Lcmol/LCH3COOH溶液与0.1molNaOH固体混合,使之充分反应。然后向该混合溶液中加入CH3COOH 或CH3COONa固体(忽略体积和温度变化),引起溶液pH的变化如图所示。下列叙述错误的是

A. 该温度下,醋酸的电离平衡常数Ka=![]()
B. a点对应的混合溶液中c(CH3COOH)>c(Na+)>c(OH-)
C. 水的电离程度:c>b>a
D. 当混合溶液呈中性时,c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.Li通常保存在煤油中,以隔绝空气
B.碱金属阳离子,氧化性最强的是Li+
C.卤素单质与水反应均可用X2+H2O![]() HXO+HX表示
HXO+HX表示
D.从Li到Cs,碱金属的密度越来越大,熔、沸点越来越高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com