
【题目】下列为四个常用的电化学装置,关于它们的叙述正确的是
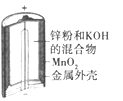
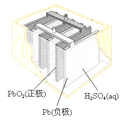
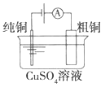
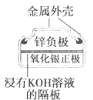
(a)碱性锌锰电池 (b)铅硫酸蓄电池 (c)电解精炼铜 (d)银锌纽扣电池
A.图(a)所示电池中,MnO2的作用是催化剂
B.图(b)所示电池放电过程中,硫酸浓度不断增大
C.图(c)所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D.图(d)所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
科目:高中化学 来源: 题型:
【题目】化学与生产生活密切相关,下列说法不正确的是( )
A. 氯气可以做杀菌消毒剂 B. 过氧化钠可以做呼吸面具的供氧剂
C. 氢氟酸可以雕刻玻璃 D. 二氧化硅可用来制造太阳能电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由KAl(SO4)2、Al2O3和Fe2O3组成的混合物A,在一定条件下可实现下图所示的物质之间的变化[说明:KAl(SO4)2可完全电离生成K+、Al3+、SO42-]:

据此回答下列问题:
(1)根据上述框图反应关系,写出下列B、D所含物质的化学式:固体B______________;沉淀D _________________。
(2)I中分离溶液和沉淀的操作是________________。
(3)写出②的离子方程式_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.铅的冶炼有很多种方法。
(1)瓦纽科夫法熔炼铅,其相关反应的热化学方程式如下:
①2PbS(s)+3O2(g)=2PbO(s)+2SO2(g) △H1= a kJmol-1
②PbS(s)+2PbO(s)=3Pb(s)+SO2(g) △H2= b kJmol-1
③PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g) △H3=c kJmol-1
反应 3PbS(s)+6O2(g)=3PbSO4(s) △H=___________kJmol-1 (用含 a、b、c 的代数式表示)。
(2)还原法炼铅,包含反应PbO(s)+CO(g)![]() Pb(s)+CO2(g) △H,该反应的平衡常数的对数值与温度的关系如下表
Pb(s)+CO2(g) △H,该反应的平衡常数的对数值与温度的关系如下表
温度/℃ | 300 | 727 | 1227 |
1gK | 6.17 | 2.87 | 1.24 |
①该反应的△H__________0(选填“ >”、“< ”或“=”)。
②当1gK=1,在恒容密闭容器中放入足量的PbO并通入CO,达平衡时,混合气体中CO的体积分数为_______________(保留两位有效数字);若平衡后再向容器中充入一定量的CO气体,平衡向_______________(填“正向”、“逆向”或“不”)移动,再次达到平衡时,CO的转化率_______________(填“增大”、“减小”或“不变”)。
Ⅱ.PbI2可用于人工降雨,可用滴定方法测出PbI2的Ksp。
(3)取一定量的PbI2固体,用蒸馏水配制成饱和溶液,准确移取25.00mL PbI2饱和溶液分次加入阳离子交换树脂RH+(发生:2RH++PbI2=R2Pb2++2H++2I-),用锥形瓶接收流出液,最后用蒸馏水淋洗树脂至流出液呈中性,将洗涤液一并转入锥形瓶中(如图)。加入酚酞指示剂,用0.0025mol·L-1NaOH溶液滴定,当达到滴定终点时,用去氢氧化钠溶液20.00mL。确定到滴定终点时锥形瓶中现象为___________________,计算PbI2的Ksp为_______________ 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾由多种污染物形成,其中包含颗粒物(包括PM2.5在内)、氮氧化物(NOx)、CO、SO2等。化学在解决雾霾污染中有着重要的作用。
(1)已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=196.6 kJ·mol1
2SO3(g) ΔH=196.6 kJ·mol1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=113.0 kJ·mol1
2NO2(g) ΔH=113.0 kJ·mol1
则反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)ΔH= kJ·mol1。
SO3(g)+NO(g)ΔH= kJ·mol1。
一定条件下,将NO2与SO2以体积比1∶2置于恒温恒容的密闭容器中发生上述反应,下列能说明反应达到平衡状态的有 。
A.体系密度保持不变
B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变
D.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1∶5,则平衡常数K= 。
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)![]() CH3OH(g)。
CH3OH(g)。
CO在不同温度下的平衡转化率与压强的关系如图所示。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。

(3)如图是一种用NH3脱除烟气中NO的原理。

①该脱硝原理中,NO最终转化为H2O和 (填化学式)。
②当消耗1 mol NH3和0.5 mol O2时,除去的NO在标准状况下的体积为 L。
(4)NO直接催化分解(生成N2和O2)也是一种脱硝途径。在不同条件下,NO的分解产物不同。在高压下,NO在40℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图所示,写出NO分解的化学方程式 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,
已知该反应中H2O2只发生如下过程:H2O2→O2。
(1)该反应中的还原剂是__________。
(2)该反应中,发生还原反应的过程是_____________________。
(3)写出该反应的化学方程式,并用单线桥或双线桥标出电子转移的方向和数目________________________________________________________
(4)若反应转移了0.3mol电子,则产生的气体在标准状况下体积为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组用镍触媒废料(主要成分为Ni-Al合金,混有少量Fe、Cu、Zn、Pb及有机物) 制备NiO并回收金属资源的流程如下所示:

已知:相关数据如表1和表2所示
表1部分难溶电解质的溶度积常数(25℃)
物质 | Ksp | 物质 | Ksp |
Fe(OH)3 | 4.0×10-38 | CuS | 6.3×10-34 |
Fe(OH)2 | 1.8×10-16 | ZnS | 1.6×10-24 |
Al(OH)3 | 1.0×10-33 | PbS | 8.0×10-28 |
Ni(OH)2 | 2.0×10-15 | NiS | 3.2×10-18 |
表2 原料价格表
物质 | 价格/(元吨-1) |
漂液(含25.2%NaClO) | 450 |
双氧水(含30%H2O2) | 2400 |
烧碱(含98%NaOH) | 2100 |
纯碱(含99.5%Na2CO3) | 600 |
请回答下列问题:
(1)“焙烧”的目的是________________________________。
(2)“试剂a”的名称为__________________;选择该试剂的理由是________________________。
(3)“氧化”时反应的离子方程式为__________________________________________。
(4)欲使溶液中Fe3+和A13+的浓度均小于等于1.0×10-6 mol L-1,需“调节pH”至少为_______________。
(5)“加水煮沸”时,反应的化学方程式为_______________________________。
(6)整个流程中,可回收的金属化合物为____________________________________(填化学式)。
(7)氢镍电池是一种应用广泛的二次电池,放电时,该电池的总反应为NiOOH+MH==Ni(OH)2+M,当导线中流过2 mol电子时,理论上负极质量减少__________g。充电时的阳极反应式为_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酸的酸式盐NaHY在水溶液中,HY-的电离程度小于HY-的水解程度。有关的叙述正确的是
A. H2Y的电离方程式为:H2Y+2H2O![]() 2H3O++Y2-
2H3O++Y2-
B. 在该酸式盐溶液中c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+)
C. HY-的水解方程式为HY-+H2O![]() H3O++Y2-
H3O++Y2-
D. 在该酸式盐溶液中c(Na+)>c(HY-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中能大量共存的一组离子或分子是( )
A. NH4+、H+、NO3-、Fe2+ B. K+ 、Al3+、SO42-- 、NH3·H2O
C. Na+、K+、SO32-、Cl2 D. Na+ 、Cl-、CO32-、OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com