
x、y为两种元素的原子,x的阴离子与y的阳离子具有相同的电子层结构,由此可知
A.x的原子半径大于y的原子半径 B.x的电负性大于y的电负性
C.x的能层数性等于y的能层数 D.x的第一电离能小于y的第一电离能
科目:高中化学 来源: 题型:
下列热化学方程式书写正确的是 )。
A.2SO2+O2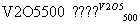 2SO3 ΔH=-196.6 kJ·mol-1
2SO3 ΔH=-196.6 kJ·mol-1
B.H2g)+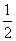 O2g)===H2Ol) ΔH=-285.8 kJ·mol-1
O2g)===H2Ol) ΔH=-285.8 kJ·mol-1
C.2H2g)+O2g)===2H2Ol) ΔH=-571.6 kJ
D.Cs)+O2g)===CO2g) ΔH=+393.5 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
硫元素有多种化合价,可形成多种化合物。
(1)旋转喷雾干燥法是去除燃煤烟气中二氧化硫的方法之一,工艺流程如下图所示,写出雾化器中发生反应的化学方程式:________________________________________________。
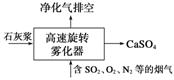
(2)已知NaHSO3溶液显弱酸性,其原因用离子方程式表示为____________。
(3)请按照浓度由大到小的顺序排列0.1 mol·L-1 Na2SO3 溶液中的离子________。Na2SO3溶液放置于空气中一段时间后,溶液的pH________(填“增大”、“减小”或“不变”)。
(4)某同学在常温下设计如下实验流程探究Na2S2O3的化学性质。
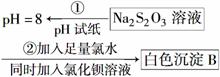
实验①可说明________(填字母)。
A.该Na2S2O3溶液中水电离的c(OH-)=10-8 mol·L-1
B.H2S2O3是一种弱酸
C.Na2S2O3是一种弱电解质
D.Na2S2O3能发生水解,其离子方程式为S2O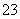 +2H2O===H2S2O3+2OH-
+2H2O===H2S2O3+2OH-
实验②说明Na2S2O3具有________性。写出发生反应的离子方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
能说明BF3分子中的4个原子处于同一平面的理由是( )
A.3个B—F的键能相同 B.3个B—F的键长相同
C.3个B—F的键角均为120° D.3个B—F的键均为σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)Li3N中氮以N3-存在,基态N3-的电子排布式为________。
(2)O=O键的键能为497.3kJ·mol-1,O—O键的键能为142kJ·mol-1,说明O2中的________键更稳定(填“σ”或“π”)。
(3)BF3与F-可形成BF4-离子。BF3与F-形成BF4-离子时,二者形成的化学键为________键。
(4)X+中所有电子正好充满K、L、M三个电子层,则X的元素符号是________,基态X+的电子排布式为_____________________________________________。
(5)与N2互为等电子体的一种分子为 (填化学式),该分子中σ键与π键的个数比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器内,发生如下反应N2+3H2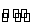 2NH3。
2NH3。
(1)若反应到某时刻t时,n(N2)=13 mol, n(NH3)=6 mol,a=_______。
(2)反应到达平衡时,混合气体体积为716.8 L(标准状况)其中NH3的含量(体积分数)为25%,计算平衡时NH3的物质的量_________。
(3)混合气体中a∶b=_________。
(4)平衡混合气体中n(N2)∶n(H2)∶n(NH3)=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组的同学通过对亚硫酸钠组成元素的价态进行分析后认为Na2SO3溶液在存放过程中有可能变质,若已变质,则相应反应的化学方程式为__________________________。
(1)甲同学设计了如下两种方案来检验Na2SO3溶液是否变质。
方案Ⅰ:取样,加入稀盐酸有气泡生成,认为Na2SO3溶液没有变质。
方案Ⅱ:取样,加入氯化钡溶液有白色沉淀生成,认为Na2SO3溶液完全变质。
乙同学认为上述两种方案均不合理,乙同学作出判断的依据分别是方案Ⅰ:________;方案Ⅱ:________。
(2)乙同学设计如图所示装置(夹持装置已略去)探究Na2SO3溶液是否变质,量取60 mL标签上注明为1.0 mol·L-1的Na2SO3溶液放入A装置中,通过测量生成的SO2质量的方法来判断其是否变质。
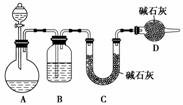
①D装置的作用是________,该实验装置中还存在一个明显的缺陷是________________,分液漏斗中应加入足量的________(填字母);
a.浓硝酸 b.65%硫酸
c.浓盐酸 d.20%硫酸
②改进缺陷后再进行实验,若实验前后测得C装置增重3.2 g,则Na2SO3变质的百分率是__________。
(3)丙同学认为若只是确定Na2SO3是否变质,乙的方案太复杂了,他认为只需要试管、胶头滴管、盐酸及氯化钡溶液就可以达到目的(不考虑对环境的影响),请你发表自己的看法(若不同意,请说明理由;若同意,请写出主要操作、现象及结论):______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com