
A.H2S B.O
 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 | 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| A | B | |
| C | D |
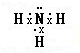
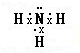
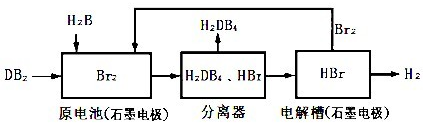
| 化学键 | H-H | Br-Br | H-Br |
| 能量(kJ/mol) | 436 | 194 | 362 |
| 化学式 | Ag2SO4 | AgBr |
| 溶解度(g) | 0.796 | 8.4×10-6 |
查看答案和解析>>
科目:高中化学 来源: 题型:


 的名称
的名称



查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江省台州市仙居县宏大中学高二(上)期中化学试卷(解析版) 题型:填空题
 的名称
的名称 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com