
下列说法正确的是()
A. 将10 g CaCO3粉末加入100 mL水中,所得溶液的浓度为l mol•L﹣1
B. 将100 mL 2 mol•L﹣1盐酸加热蒸发至50 mL,所得溶液的浓度为4 mol•L﹣1
C. 将l0 mL l.0mol•L﹣1NaCl溶液与90mL水混合,所得溶液的浓度为0.1 mol•L﹣1
D. 将10 g CaO加入100 mL饱和石灰水中,充分搅拌、静置并恢复到原来的温度,所得溶液的浓度不变
考点: 物质的量浓度的相关计算.
专题: 物质的量浓度和溶解度专题.
分析: A.碳酸钙为难溶物,所以溶解的碳酸钙的物质的量远远小于0.1mol;
B.氯化氢具有挥发性,加热过程中溶质的物质的量减小,则溶液浓度小于4mol/L;
C.混合液体积不是100mL,则溶液浓度不是0.1mol/L;
D.温度不变,反应后仍然为氢氧化钙饱和溶液,则其浓度不变.
解答: 解:A.将10 g CaCO3粉末加入100 mL水中,由于碳酸钙难溶于水,则所得溶液的浓度远远小于l mol•L﹣1,故A错误;
B.将100 mL 2 mol•L﹣1盐酸加热蒸发至50 mL,加热过程中氯化氢挥发,则所得溶液的浓度小于4 mol•L﹣1,故B错误;
C.将l0 mL l.0mol•L﹣1NaCl溶液与90mL水混合,混合液体积不能简单加和,则所得溶液的浓度不是0.1 mol•L﹣1,故C错误;
D.10 g CaO加入100 mL饱和石灰水中,充分搅拌、静置并恢复到原来的温度,所得溶液仍然为氢氧化钙饱和溶液,溶液具有均一性,则溶液的浓度不变,故D正确;
故选D.
点评: 本题考查了物质的量浓度的计算,题目难度中等,注意掌握物质的量浓度的概念及计算方法,明确溶液具有均一性特点,特别是计算混合液体积时,没有说明时不能将溶液体积简单加和.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
高锰酸钾在不同的条件下发生的反应如下:
MnO4﹣+5e﹣+8H+═Mn2++4H2O①
MnO4﹣+3e﹣+2H2O═MnO2↓+4OH﹣②
MnO4﹣+e﹣═MnO42﹣(溶液绿色)③
(1)从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的酸碱性影响.
(2)将SO2通入高锰酸钾溶液中,发生还原反应的离子反应过程为 ﹣→ +.
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色.下列说法正确的
a.氧化性:PbO2>KMnO4
b.还原性:PbO2>KMnO4
c.该反应可以用盐酸酸化
(4)将高锰酸钾逐滴加入到硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量之比为3:2,完成下列化学方程式(横线上填系数,括号内填物质):
KMnO4+ K2S+ KOH═ K2MnO4+3K2SO4+2S↓+ .
②若生成6.4g单质硫,反应过程中转移电子的物质的量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
配制100mL 1.0mol/LNa2CO3溶液,下列操作正确的是()
A. 称取10.6g无水碳酸钠,加入100mL容量瓶中,加水溶解、定容
B. 称取10.6g无水碳酸钠,加入100mL蒸馏水,搅拌、溶解
C. 转移Na2CO3溶液时,未用玻璃棒引流,直接倒入容量瓶中
D. 定容后,塞好瓶塞,反复倒转、摇匀
查看答案和解析>>
科目:高中化学 来源: 题型:
现有下列短周期元素性质的数据:
元素编号
元素性质 ① ② ③ ④ ⑤ ⑥ ⑦ ⑧
原子半径 0.74 1.60 1.52 1.10 0.99 1.86 0.75 0.82
最高或最低化合价 +2 +1 +5 +7 +1 +5 +3
﹣2 ﹣3 ﹣1 ﹣3
下列说法正确的是()
A. 原子序数④元素大于⑦元素
B. ②、③处于同一周期
C. 上述八种元素最高价氧化物对应的水化物,⑤号酸性最强
D. ⑧号元素原子结构示意图为:
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是温度和压强对反应X+Y⇌2Z影响的示意图.下列叙述正确的是()
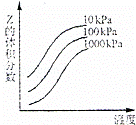
A. 该反应为放热反应
B. 增大压强,平衡正向移动
C. X、Y、Z均为气态
D. X和Y中只有一种为气态,Z为气态
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室可用NaNO2+NH4Cl═NaCl+N2↑+2H2O制备N2,下列说法正确的是()
A. NaNO2发生氧化反应
B. NH4Cl中的氮元素被还原
C. N2既是氧化产物,又是还原产物
D. 每生成1mol N2转移电子的物质的量为6mol
查看答案和解析>>
科目:高中化学 来源: 题型:
a、b、c、d、e是含有一种相同元素的五种物质,可发生如图转化:其中:a是单质;b是气体;c、d是氧化物;e是最高价氧化物对应的水化物.
(1)如果a是一种淡黄色粉末固体,试推断这五种物质(用名称表示):
A ;b ;c ;d ;e .
并写出由c生成d的化学方程式
(2)如果a为单质且是一种常见气体,试推断这五种物质(用化学式表示):
A ;b ;c ;d ;e .
并写出由d生成e的化学方程式 .
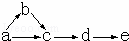
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数,下列说法中正确的是( )
|
| A. | 1NA个氢气分子所占的体积为22.4L |
|
| B. | 2NA个二氧化碳分子的质量为44g |
|
| C. | 1000mL0.1mol/L的NaCl溶液中,Na+与Cl﹣离子总数为0.2NA |
|
| D. | 17g氨气中所含原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列事实不能说明上述观点的是()
A. 苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应
B. 乙烯能发生加成反应,乙烷不能发生加成反应
C. 甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色
D. 苯与硝酸在加热时发生取代反应,甲苯与硝酸在常温下就能发生取代反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com