
下列关于自然界中氮循环(如右图)的说法不正确的是:
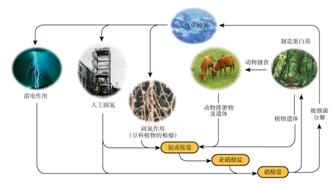
A.但元素均被氧化
B.工业合成氨属于人工固氮
C.含氮无机物和含氮有机物可相互转化
D.碳、氢、氧三种元素也参与了氮循环
 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:
下列有关化学用语使用正确的是 ( )
A.硫原子的原子结构示意图: B.NH4Cl的电子式:
B.NH4Cl的电子式: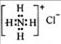
C.N2的结构式::N≡N: D.原子核内有10个中子的氧原子: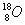
查看答案和解析>>
科目:高中化学 来源: 题型:
顺丁橡胶、制备醇酸树脂的原料M以及杀菌剂N的合成路线如下:
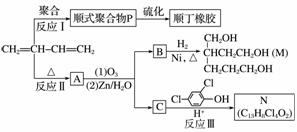
已知:ⅰ.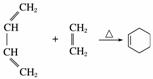
ⅱ.RCH===CHR′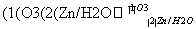 RCHO+R′CHO(R、R′代表烃基或氢)
RCHO+R′CHO(R、R′代表烃基或氢)
(1)CH2===CH—CH===CH2的名称是______________。
(2)反应Ⅰ的反应类型是(选填字母)________。
a.加聚反应 b.缩聚反应
(3)顺式聚合物P的结构式是(选填字母)________。
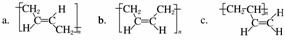
(4)A的相对分子质量为108。
①反应Ⅱ的化学方程式是___________________________________________________。
②1 mol B完全转化成M所消耗H2的质量是______g。
(5)反应Ⅲ的化学方程式是_______________________________________________________。
(6)A的某些同分异构体在相同的反应条件下也能生成B和C。写出其中一种同分异构体的结构简式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述Ⅰ和Ⅱ均正确并有因果关系的是
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 1-己醇的沸点比己烷的沸点高 | 1-己醇和己烷可通过蒸馏初步分离 |
| B | 原电池可将化学能转化为电能 | 原电池需外接电源才能工作 |
| C | 乙二酸可与KMnO4溶液发生反应 | 乙二酸具有酸性 |
| D | Na在Cl2中燃烧的生成物含离子键 | NaCl固体可导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
用O2将HCl转化为Cl2,可提高效益,减少污染,
(1)传统上该转化通过如右图所示的催化剂循环实现,

其中,反应①为:2HCl(g) + CuO(s) 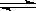 H2O(g)+CuCl2(g) △H1
H2O(g)+CuCl2(g) △H1
反应②生成1molCl2 (g)的反应热为△H2,则总反应的热化学方程式
(g)的反应热为△H2,则总反应的热化学方程式
为 , (反应热用△H1和△H2表示)。
(2)新型RuO2催化剂对上述HCl转化为Cl2的总反应具有更好的催化活性,
①实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的ɑHCl—T曲线如图12,
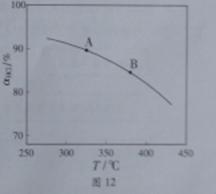
则总反应的△H 0 ,(填“>”、“﹦”或“<”);A、B两点的平衡常数K(A)与K(B)中较大的是 。
②在上述实验中若压缩体积使压强增大,画出相应ɑHCl—T曲线的示意图,并简要说明理由: 。
③下列措施中有利于提高ɑHCl的有 。
 A、增大n(HCl) B、增大n(O2)
A、增大n(HCl) B、增大n(O2)
C、 使用更好的催化剂 D、移去H2O
使用更好的催化剂 D、移去H2O
(3)一定条件下测得反应过程中n(Cl 2)的数据如下:
2)的数据如下:
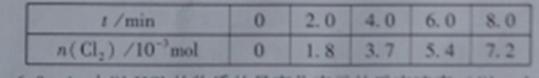
计算2.0~6.0min内以HCl的物质的量变化表示的反应速率(以mol·min-1为单位,写出计算过程)。
(4)Cl2用途 广泛,写出用Cl2制备漂白粉的化学方程式。
广泛,写出用Cl2制备漂白粉的化学方程式。
查看答案和解析>>
科目:高中化学 来源: 题型:
“张-烯炔环异构反应”被《Name Reactions》收录。该反应可高效构筑五元环化合物:

(R、R‘、R“表示氢、烷基或芳基)
合成五元环有机化合物J的路线如下:
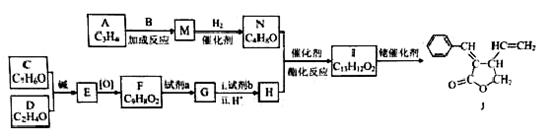
已知: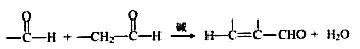
(1)A属于炔烃,其结构简式是 。
(2)B由碳、氢、氧三种元素组成,相对分子质量是30。B的结构简式是
(3)C、D含有与B相同的官能团,C是芳香族化合物,E中含有的官能团是
(4)F与试剂a反应生成G的化学方程式是 ;试剂b是 。
(5)M和N均为不饱和醇。M的结构简式是
(6)N为顺式结构,写出N和H生成I(顺式结构)的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关NaClO和NaCl混合溶液的叙述正确的是:
A.该溶液中,H+、NH4+、SO42-、Br-可以大量共存
B.该溶液中,Ag+、K+、NO3-、CH3CHO可以大量共存
C.向该溶液中滴入少量FeSO4溶液,反应的离子方程式为:
2Fe2++ClO-+2H+=== Cl-+2Fe3++H2O
D.向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个
查看答案和解析>>
科目:高中化学 来源: 题型:
FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小。请回答下列问题:
(1)FeCl3 净水的原理是 。FeCl3 溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示) 。
(2)为节约成本,工业上用NaClO3 氧化酸性FeCl2 废液得到FeCl3 。
①若酸性FeCl2 废液中c(Fe2+)=2.0×10-2mol·L-1, c(Fe3+)=1.0×10-3mol·L-1, c(Cl-)=5.3×10-2mol·L-1,则该溶液的PH约为 。
②完成NaClO3 氧化FeCl2 的离子方程式:
| |
 ClO3-+
ClO3-+
|
 Fe2++
Fe2++ | |
 =
= | |
 Cl-+
Cl-+ | |
 Fe3++
Fe3++ | |
 .
. (3)FeCl3 在溶液中分三步水解:
Fe3++H2O  Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是 。
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:
xFe3++yH2O Fex(OH)y(3x-y)++yH+
Fex(OH)y(3x-y)++yH+
 欲使平衡正向移动可采用的方法是(填序号) 。
欲使平衡正向移动可采用的方法是(填序号) 。
a.降温 b.加水稀释 c.加入NH4Cl d.加入NaHCO3
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是 。
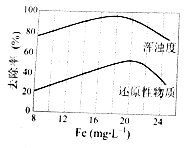
(4)天津某污水处理厂用氯化铁净化污水的结果如下图所示。由图中数据得出每升污水中投放聚合氯化铁[以Fe(mg·L-1)表示]的最佳范围约为 mg·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
浙江大学成功研制出能在数分钟之内将电量充满的锂电池,其成本只有传统锂电池的一半。若电解液为LiAlCl4-SOCl2,电池的总反应为:4Li+2SOCl2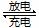 4LiCl+S+SO2。下列说法不正确的是
4LiCl+S+SO2。下列说法不正确的是
A.Li为电池的负极
B.电池的电解液可用LiCl水溶液代替
C.放电时电子从负极经外电路流向正极
D.充电时阳极反应式为:4Cl-+S+SO2-4e-=2SOCl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com