
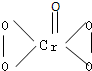
 ?
?| a | b | ||||||||||||||||
| c | d | ||||||||||||||||
| e | f | g | h | ||||||||||||||
| i | j | ||||||||||||||||
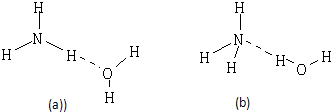
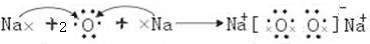
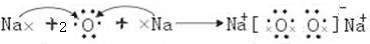
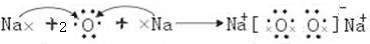 ,
,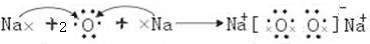 ;
;

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
据报道双氧水接触银能剧烈反应,为消除用硝酸清洗试管内壁上的银时产生的有毒气体污染环境,体现“绿色化学”的理念,某学校活动小组利用该反应清洗试管内壁上的银,并进一步研究反应的机理。他们查阅资料(资料信息:硝酸氧化性比过氧化氢强,能氧化过氧化氢;碘化银为黄色固体;稀硝酸与银单质反应条件为加热),设计并完成了以下实验。
第一步 清洗: 取10 mL 10% H2O2溶液清洗附有银的试管。反应剧烈,并产生大量的气体(经验证为氧气),试管内壁上的银全部被清除干净,最后得澄清透明液体a。用激光照射液体a能看到丁达尔效应。
第二步 探究反应原理: 取2支试管,分别取液体a约1 mL,稀释至3 mL得液体b。
学生甲:将1支盛有液体b的试管进行如下实验

学生乙:向液体b中加入4~5滴稀硝酸酸化的2 mol/LNaCl溶液,溶液中出现白色沉淀。
通过上述实验,他们认为H2O2氧化了银单质。请回答:
(1)液体a在分散系分类中属于 。
(2)操作x名称是 。
(3)学生甲在液体b中加入碘化钾溶液,没有看到预期的黄色的碘化银沉淀,可能的原因是 (填序号)。
①液体a中的银元素大多数以银单质的形式存在
②过量的H2O2将I—氧化为I2
③加入的碘化钾溶液量太少
(4)学生乙在实验中加入4~5滴稀硝酸酸化的原因是 。
(5)如果银与H2O2反应生成的物质对H2O2的分解有催化作用,通过分析可以推测,起催化作用的物质是
查看答案和解析>>
科目:高中化学 来源:2010-2011学年辽宁省丹东市四校协作体第二次联考高三化学试卷 题型:实验题
据报道双氧水接触银能剧烈反应,为消除用硝酸清洗试管内壁上的银时产生的有毒气体污染环境,体现“绿色化学”的理念,某学校活动小组利用该反应清洗试管内壁上的银,并进一步研究反应的机理。他们查阅资料(资料信息:硝酸氧化性比过氧化氢强,能氧化过氧化氢;碘化银为黄色固体;稀硝酸与银单质反应条件为加热),设计并完成了以下实验。
第一步 清洗: 取10 mL 10% H2O2溶液清洗附有银的试管。反应剧烈,并产生大量的气体(经验证为氧气),试管内壁上的银全部被清除干净,最后得澄清透明液体a。用激光照射液体a能看到丁达尔效应。
第二步 探究反应原理: 取2支试管,分别取液体a约1 mL,稀释至3 mL得液体b。
学生甲:将1支盛有液体b的试管进行如下实验

学生乙:向液体b中加入4~5滴稀硝酸酸化的2 mol/LNaCl溶液,溶液中出现白色沉淀。
通过上述实验,他们认为H2O2氧化了银单质。请回答:
(1)液体a在分散系分类中属于 。
(2)操作x名称是 。
(3)学生甲在液体b中加入碘化钾溶液,没有看到预期的黄色的碘化银沉淀,可能的原因是 (填序号)。
①液体a中的银元素大多数以银单质的形式存在
②过量的H2O2将I—氧化为I2
③加入的碘化钾溶液量太少
(4)学生乙在实验中加入4~5滴稀硝酸酸化的原因是 。
(5)如果银与H2O2反应生成的物质对H2O2的分解有催化作用,通过分析可以推测,起催化作用的物质是
查看答案和解析>>
科目:高中化学 来源:2010年广西南宁三中高考化学二轮复习卷(解析版) 题型:填空题
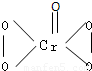 ?
?| a | b | ||||||||||||||||
| c | d | ||||||||||||||||
| e | f | g | h | ||||||||||||||
| i | j | ||||||||||||||||
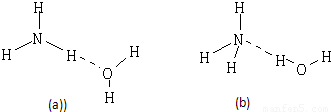
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com