
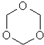
 ),三聚甲醛可用作合成工程塑料等,还是日用化妆品冷烫精及脱毛剂的主要原料.下列有关三聚甲醛的说法中正确的是( )
),三聚甲醛可用作合成工程塑料等,还是日用化妆品冷烫精及脱毛剂的主要原料.下列有关三聚甲醛的说法中正确的是( )| A. | 三聚甲醛属于高分子化合物 | |
| B. | 三聚甲醛与甘油互为同分异构体 | |
| C. | 三分子甲醛合成三聚甲醛的反应属于加成反应 | |
| D. | 1 mol的三聚甲醛燃烧时生成CO2和H2O的物质的量一定相等 |
分析 A.高分子化合物相对分子质量在10000以上;
B.分子式相同结构不同的有机物互为同分异构体;
C.三分子甲醛合成三聚甲醛的反应属于加成反应;
D.三聚甲醛的分子式为C3H6O3,根据原子守恒判断.
解答 解:A.高分子化合物相对分子质量在10000以上,该分子相对分子质量较小,所以不属于高分子化合物,故A错误;
B.分子式相同结构不同的有机物互为同分异构体,丙三醇分子式为C3H8O3,三聚甲醛分子式为C3H6O3,所以不是同分异构体,故B错误;
C.该反应符合加成反应特点,所以属于加成反应,故C正确;
D.三聚甲醛的分子式为C3H6O3,根据原子守恒知,如果完全燃烧生成二氧化碳和水的物质的量相等,如果生成CO,则生成的二氧化碳和水的物质的量不等,故D错误;
故选C.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系、物质结构特点及基本概念是解本题关键,易错选项是D,易忽略不完全燃烧而导致错误.


科目:高中化学 来源: 题型:解答题
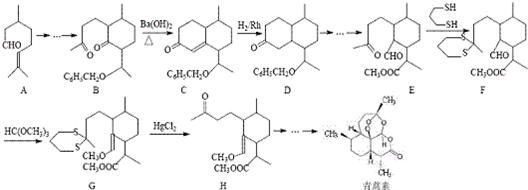
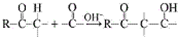
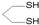 用系统命名法命名,它的名称是1,3-丙二硫醇;反应B→C,实际上可看作两步进行,依次发生的反应类型是加成反应、消去反应.
用系统命名法命名,它的名称是1,3-丙二硫醇;反应B→C,实际上可看作两步进行,依次发生的反应类型是加成反应、消去反应.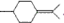 ,则异蒲勒醇的结构简式为:
,则异蒲勒醇的结构简式为: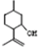 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素的化学性质随着相对原子质量的递增而呈周期性变化 | |
| B. | 元素的最外层电子数等于元素的最高化合价 | |
| C. | 原子序数越大,原子半径越大 | |
| D. | 元素周期律是元素原子核外电子排布周期性变化的结果 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24LCHCl3中含有碳氯键数目为0.3NA | |
| B. | 25℃时,0.1mol/L的Na2CO3溶液中含有Na+的数目为0.02NA | |
| C. | 28gN2和CO的混合气体中含有的分子数为NA | |
| D. | 1molNa2O和1molNa2O2的混合物中,含有的离子总数为7NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
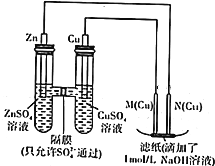 用如图示装置进行实验
用如图示装置进行实验查看答案和解析>>
科目:高中化学 来源: 题型:解答题
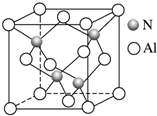 某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域.
某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
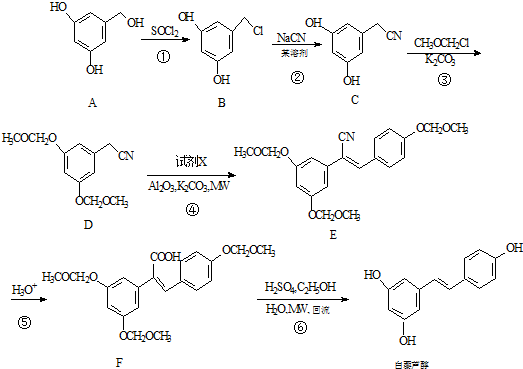
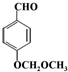 .
.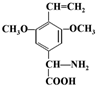 或
或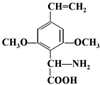 .(任写一种)
.(任写一种)查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 塑料 | B. | 玻璃 | C. | 淀粉 | D. | 合成纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
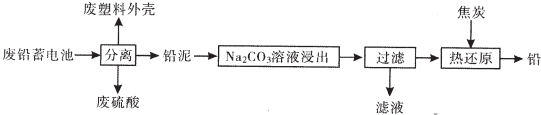
| 物质 | Kap(25℃) | 颜色 |
| PbSO4 | 1.8×10-8 | 白色 |
| PbCO3 | 1.5×10-13 | 白色 |
| PbCrO4 | 1.8×10-14 | 黄色 |
| BaCrO4 | 1.2×10-10 | 黄色 |
| Pb(OH)2 | 1.8×10-20 | 白色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com