
 ����һ�ֿ����ھ�ˮ����ʳƷ���Σ���A��B��C��D��E���ֶ�����Ԫ����ɣ�������ˮ��ɵ�����������ӣ�����һ������A��B�γɵ�10���������ӣ�AԪ��ԭ�Ӻ�����������E����l��D��Eͬ���壮ijͬѧΪ̽������ɶ���������ʵ�飺
����һ�ֿ����ھ�ˮ����ʳƷ���Σ���A��B��C��D��E���ֶ�����Ԫ����ɣ�������ˮ��ɵ�����������ӣ�����һ������A��B�γɵ�10���������ӣ�AԪ��ԭ�Ӻ�����������E����l��D��Eͬ���壮ijͬѧΪ̽������ɶ���������ʵ�飺���� ����A��B��C��D��E���ֶ�����Ԫ����ɵ�һ���Σ���ȡ��������Һ���Թ��У���ε���Ba��OH��2��Һ�����ɳ�����ʼ���������С�����������ղ���ȫ��ʧ�������Һ�϶�����SO42-��Al3+����ȡ20mL����Һ���Թ��У��������NaOH��Һ����Ȳ��ռ����������壬�����Һ�к���NH4+�������ڵ��봦���������ӣ�A��B�γɵ�10����������ΪNH4+��D��Eͬ���壬����Ӧ�γ�SO42-����AԪ��ԭ�Ӻ�����������E����l����AΪNԪ�ء�EΪOԪ�ء�DΪSԪ�ء�BΪHԪ�ء�CΪAl����2���о��ⶨ�����Ħ������Ϊ453g��mol-1����1mol�����к���12mol�ᾧˮ�����������Ӻ������ӵķ�����Ϊ��453-216=237�������Ӻ����������ʵ���֮��1��1�����ݵ�����ԭ�����仯ѧʽΪ��NH4Al��SO4��2•12H2O��oa�η�����Ӧ��2NH4Al��SO4��2+3Ba��OH��2=3BaSO4��+2Al��OH��3��+��NH4��2SO4��ab�η�����Ӧ����NH4��2SO4+Ba��OH��2=BaSO4��+2NH3��H2O��bc�η�����Ӧ��OH-+Al��OH��3=AlO2-+2H2O���ݴ˽��
��� �⣺����A��B��C��D��E���ֶ�����Ԫ����ɵ�һ���Σ���ȡ��������Һ���Թ��У���ε���Ba��OH��2��Һ�����ɳ�����ʼ���������С�����������ղ���ȫ��ʧ�������Һ�϶�����SO42-��Al3+����ȡ20mL����Һ���Թ��У��������NaOH��Һ����Ȳ��ռ����������壬�����Һ�к���NH4+�������ڵ��봦���������ӣ�A��B�γɵ�10����������ΪNH4+��D��Eͬ���壬����Ӧ�γ�SO42-����AԪ��ԭ�Ӻ�����������E����l����AΪNԪ�ء�EΪOԪ�ء�DΪSԪ�ء�BΪHԪ�ء�CΪAl����2���о��ⶨ�����Ħ������Ϊ453g��mol-1����1mol�����к���12mol�ᾧˮ�����������Ӻ������ӵķ�����Ϊ��453-216=237�������Ӻ����������ʵ���֮��1��1�����ݵ�����ԭ�����仯ѧʽΪ��NH4Al��SO4��2•12H2O��oa�η�����Ӧ��2NH4Al��SO4��2+3Ba��OH��2=3BaSO4��+2Al��OH��3��+��NH4��2SO4��ab�η�����Ӧ����NH4��2SO4+Ba��OH��2=BaSO4��+2NH3��H2O��bc�η�����Ӧ��OH-+Al��OH��3=AlO2-+2H2O��
��1��DΪSԪ�أ��������ڱ��е�������VIA�壬
�ʴ�Ϊ����������VIA�壻
��2��������������֪���Ļ�ѧʽΪ��NH4Al��SO4��2•12H2O��
�ʴ�Ϊ��NH4Al��SO4��2•12H2O��
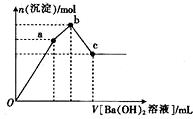
��3������NH4Al��SO4��2•12H2OΪ2mol��oa�η�����Ӧ��2NH4Al��SO4��2+3Ba��OH��2=3BaSO4��+2Al��OH��3��+��NH4��2SO4������3molBa��OH��2������1mol��NH4��2SO4������2molAl��OH��3��ab�η�����Ӧ����NH4��2SO4+Ba��OH��2=BaSO4��+2NH3��H2O��1mol��NH4��2SO4����1molBa��OH��2��bc�η�����Ӧ��OH-+Al��OH��3=AlO2-+2H2O��2molAl��OH��3����1molBa��OH��2����ͼ����V��Oa����V��ab����V��bc��=3mol��1mol��1mol=3��1��1��
�ʴ�Ϊ��3��1��1��
��4��ab�η�����Ӧ����NH4��2SO4+Ba��OH��2=BaSO4��+2NH3��H2O�����ӷ���ʽΪ��2NH4++SO42-+Ba2++2OH-=BaSO4��+2NH3��H2O��
�ʴ�Ϊ��2NH4++SO42-+Ba2++2OH-=BaSO4��+2NH3��H2O��
��5��ʵ�����ȡ20mL����Һ���Թ��У��������NaOH��Һ����Ȳ��ռ������İ���Ϊ$\frac{0.224L}{22.4L/mol}$=0.01mol����NH4Al��SO4��2Ϊ0.01mol������ҺŨ��Ϊ$\frac{0.01mol}{0.02L}$=0.5mol/L��
�ʴ�Ϊ��0.5mol/L��
���� ���⿼��������ƶϣ��ؼ��Ǹ���ʵ�������ƶϺ��е�������ȷ���η����ķ�Ӧ���Ƕ�ѧ���ۺ������Ŀ��飬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѧ���ȴ���������ԭ��֮�䣬�ִ��������ڷ���֮�� | |
| B�� | �Ǽ��Լ�ֻ������˫ԭ�ӵĵ��ʷ����� | |
| C�� | ����ԭ��֮���ǿ����� | |
| D�� | ���ۼ�ֻ�ܴ����ڹ��ۻ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ҵ����ױ��������� | B�� | �������Ȼ�̼����ϩ | ||
| C�� | �����ױ��������� | D�� | �����������屽������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ƾ����׳�â����������ֽ����Ҫԭ�� | |
| B�� | �����ʯ��ˮ�еμ�̼������Һ�а�ɫ�������μ�̼�������ް�ɫ���� | |
| C�� | ��������һ��ũҩ����ɱ����º��� | |
| D�� | ̼�����Ʋ��ʺϸ�θ������ʹ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ȼ����Ũ�� | |
| B�� | ��ʹKMnO4������Һ��ɫ | |
| C�� | �����巢��1��2�ӳɷ�Ӧ | |
| D�� | ��������ˮ��Ӧ����������ֻ��2��̼ԭ��������ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 8��13 | B�� | 1��1 | C�� | 13��8 | D�� | 1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ʱ����ʯ���� | B�� | ���������ƹ�������ձ��г��� | ||
| C�� | ����Ͳ���ܽ��Ȼ��ƹ��� | D�� | ��pH��ֽ�������Һ�вⶨpH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�22.4L��CCl4�к�CCl4������ΪNA | |
| B�� | 5.6g ����6.4g ͭ�ֱ���0.1mol ������ȫ��Ӧ��ת�Ƶĵ�������� | |
| C�� | 0.1mol•L-1MgCl2��Һ�к�Cl-��Ϊ0.2NA | |
| D�� | 3.9g Na2O2�����к��е���������Ϊ0.2NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com