
 £®
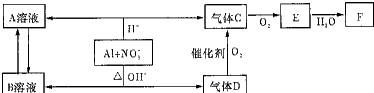
£®·ÖĪö ½šŹōĀĮŌŚĖįŠŌ»ņ¼īŠŌČÜŅŗÖŠ¾łæÉÓėNO3-·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬ÓÉ×Ŗ»Æ¹ŲĻµĶ¼æÉÖŖ£¬ŌŚĖįŠŌ»·¾³ĻĀ£¬·“Ӧɜ³ÉĀĮŃĪŗĶŅ»Ńõ»ÆµŖ£¬¼īŠŌ»·¾³ĻĀÉś³ÉĘ«ĀĮĖįŃĪŗĶ°±Ęų£¬°±Ęų“ß»ÆŃõ»ÆæÉŅŌÉś³ÉŅ»Ńõ»ÆµŖŗĶĖ®£¬Ņ»Ńõ»ÆµŖæÉŅŌŗĶŃõĘų·“Ӧɜ³É¶žŃõ»ÆµŖ£¬¹ŹAĪŖĻõĖįĀĮ£¬BĪŖĘ«ĀĮĖįŃĪ£¬CĪŖNO£¬DĪŖ°±Ęų£¬EĪŖ¶žŃõ»ÆµŖ£¬FĪŖĻõĖį£¬Č»ŗó½įŗĻŌŖĖŲ»ÆŗĻĪļŠŌÖŹ¼°»ÆѧÓĆÓļĄ“½ā“š£®
½ā“š ½ā£ŗ½šŹōĀĮŌŚĖįŠŌ»ņ¼īŠŌČÜŅŗÖŠ¾łæÉÓėNO3-·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬ÓÉ×Ŗ»Æ¹ŲĻµĶ¼æÉÖŖ£¬ŌŚĖįŠŌ»·¾³ĻĀ£¬·“Ӧɜ³ÉĀĮŃĪŗĶŅ»Ńõ»ÆµŖ£¬¼īŠŌ»·¾³ĻĀÉś³ÉĘ«ĀĮĖįŃĪŗĶ°±Ęų£¬°±Ęų“ß»ÆŃõ»ÆæÉŅŌÉś³ÉŅ»Ńõ»ÆµŖŗĶĖ®£¬Ņ»Ńõ»ÆµŖæÉŅŌŗĶŃõĘų·“Ӧɜ³É¶žŃõ»ÆµŖ£¬¹ŹAĪŖĻõĖįĀĮ£¬BĪŖĘ«ĀĮĖįŃĪ£¬CĪŖNO£¬DĪŖ°±Ęų£¬EĪŖ¶žŃõ»ÆµŖ£¬FĪŖĻõĖį£¬
£Ø1£©æÉČÜŠŌµÄĀĮŃĪæÉŅŌŗĶĘ«ĀĮĖįŃĪ·¢Éś·“Ӧɜ³ÉĒāŃõ»ÆĀĮ°×É«³Įµķ£¬·¢Éś6H2O+3AlO2-+Al3+=4Al£ØOH£©3”ż£¬¹Ź“š°øĪŖ£ŗAl£ØOH£©3£»
£Ø2£©°±ĘųæÉŅŌŗĶŅ»Ńõ»ÆµŖ»ņŹĒ¶žŃõ»ÆµŖ·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³ÉĪŽ¶¾ĘųĢåµŖĘų£¬µŖĘųŹĒµŖŌ×ÓÖ®¼äĶعż¹²ÓƵē×Ó¶ŌŠĪ³ÉµÄµ„ÖŹ£¬µē×ÓŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø3£©½šŹōĀĮŌŚ¼īŠŌ»·¾³ĻĀæÉŅŌŗĶĻõĖįøś·“Ӧɜ³ÉĘ«ĀĮĖįŃĪŗĶ°±Ęų£¬Óɵē×Ó”¢µēŗÉŹŲŗćæÉÖŖ£¬Ąė×Ó·“Ó¦ĪŖ8Al+3NO3-+5OH-+2H2O=8AlO2-+3NH3”ü£¬
¹Ź“š°øĪŖ£ŗ8£»3£»5£»2£»8AlO2-£»3NH3£»
£Ø4£©¹żĮæDČÜŅŗÓėAČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ3NH3£®H2O+Al3+=Al£ØOH£©3”ż+3NH4+£¬¹Ź“š°øĪŖ£ŗ3NH3£®H2O+Al3+=Al£ØOH£©3”ż+3NH4+£»
¶žŃõ»ÆµŖæÉŅŌŗĶĖ®·¢Éś·“Ӧɜ³ÉĻõĖįŗĶŅ»Ńõ»ÆµŖ£¬3NO2+H2OØT2HNO3+NO£¬æÉŅŌÓĆĖ®³żČ„Ņ»Ńõ»ÆµŖÖŠµÄ¶žŃõ»ÆµŖ£¬¹Ź“š°øĪŖ£ŗ3NO2+H2OØT2HNO3+NO£»
£Ø5£©D”śC·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ4NH3+5O2$\frac{\underline{“߻ƼĮ}}{”÷}$4NO+6H2O£¬¹Ź“š°øĪŖ£ŗ4NH3+5O2$\frac{\underline{“߻ƼĮ}}{”÷}$4NO+6H2O£»
£Ø6£©¶žŃõ»ÆµŖÓėĖ®·“Ӧɜ³ÉNO£¬ŌņĄūÓĆĖ®Ļ“ĘųæɳżŌÓ£¬¼“³żČ„ĘųĢåCÖŠµÄŌÓÖŹĘųĢåEµÄ»Æѧ·½·ØĪŖ3NO2+H2O=2HNO3+NO£¬¹Ź“š°øĪŖ£ŗ3NO2+H2O=2HNO3+NO£»
£Ø7£©AlÓėNO3-ŌŚĖįŠŌĢõ¼žĻĀ·“Ó¦£¬½šŹōĀĮ±»Ńõ»ÆĪŖČż¼ŪµÄĀĮĄė×Ó£¬Ź§Č„µē×Ó3mol£¬ĻõĖįøł±»»¹ŌĪŖŅ»Ńõ»ÆµŖ£¬µĆµ½µē×ÓŅ²ŹĒ3mol£¬øł¾Żµē×ÓŹŲŗć£¬AlÓė±»»¹ŌµÄNO3-µÄĪļÖŹµÄĮæÖ®±ČŹĒ1£ŗ1£¬¹Ź“š°øĪŖ£ŗ1£ŗ1£®
µćĘĄ ±¾Ģāæ¼²éĪŽ»śĪļµÄĶʶĻ£¬ĪŖøßĘµæ¼µć£¬²ąÖŲAl¼°Ęä»ÆŗĻĪļ×Ŗ»ÆµÄ漲飬°ŃĪÕ·¢ÉśµÄŃõ»Æ»¹Ō·“Ó¦ĶʶĻø÷ĪļÖŹĪŖ½ā“šµÄ¹Ų¼ü£¬ĢāÄæ×ŪŗĻŠŌ½ĻĒ棬ÄѶČÖŠµČ£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C£Øs£©+O2£Øg£©ØTCO£Øg£©”÷H=110.5 kJ/mol | |
| B£® | C£Øs£©+O2£Øg£©ØTCO2£Øg£©”÷H=-393.5 kJ/mol | |
| C£® | 2H2£Øg£©+O2£Øg£©ØT2 H2O£Øl£©”÷H=-571.6 kJ/mol | |
| D£® | H2£Øg£©+O2£Øg£©ØTH2O£Øg£©”÷H=-241.8 kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 Õė¶ŌĶųĀēÉĻĮ÷“«µÄøōŅ¹ŹģČāÖŠŅņŃĒĻõĖįÄĘ£ØNaNO2£©ŗ¬ĮæŃĻÖŲ³¬±ź¶ų²»ÄÜŹ³ÓƵÄĖµ·Ø£¬Ä³ŠĖȤŠ”×éæŖÕ¹ČēĻĀĢ½¾æ»ī¶Æ£ŗ
Õė¶ŌĶųĀēÉĻĮ÷“«µÄøōŅ¹ŹģČāÖŠŅņŃĒĻõĖįÄĘ£ØNaNO2£©ŗ¬ĮæŃĻÖŲ³¬±ź¶ų²»ÄÜŹ³ÓƵÄĖµ·Ø£¬Ä³ŠĖȤŠ”×éæŖÕ¹ČēĻĀĢ½¾æ»ī¶Æ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ö²ĪļÓĶ²»ÄÜ·¢ÉśĖ®½ā·“Ó¦ | |
| B£® | µķ·ŪĖ®½āµÄ×īÖÕ²śĪļŹĒĀóŃæĢĒ | |
| C£® | ÕįĢĒĖ®½ā²śĪļÖ»ÓŠĘĻĢŃĢĒ | |
| D£® | µ°°×ÖŹČÜŅŗÓöCuSO4ŗó²śÉśµÄ³ĮµķÖĆÓŚĖ®ÖŠ²»ÄÜÖŲŠĀČܽā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŖĖŲBµÄ»ÆŗĻĪļæÉŅŌÓĆĄ“×öŃ껚²ÄĮĻ | |
| B£® | »ÆŗĻĪļAEÓėCEŗ¬ÓŠĻąĶ¬ĄąŠĶµÄ»Æѧ¼ü | |
| C£® | ¹¤ŅµÉĻ³£ÓƵē½ā·ØÖʱøŌŖĖŲC”¢D”¢EµÄµ„ÖŹ | |
| D£® | ŌŖĖŲB”¢DµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļÖ®¼äæÉÄÜ·¢Éś·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
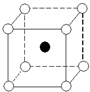 ČēĶ¼ŹĒĀČ»Æļ¤¾§ĢåµÄ¾§°ū½į¹¹Ź¾ŅāĶ¼£Ø¾§°ūŹĒÖø¾§ĢåÖŠ×īŠ”µÄÖŲø“µ„ŌŖ£©£¬ĘäÖŠŗŚĒņ±ķŹ¾ĀČĄė×Ó”¢°×Ēņ±ķŹ¾ļ¤Ąė×Ó£®ŅŃÖŖ¾§ĢåÖŠ2øö×ī½üµÄļ¤Ąė×ÓµÄŗĖ¼ä¾ąĄėĪŖa cm£¬ĀČ»Æļ¤µÄĦ¶ūÖŹĮæĪŖM g/mol£¬ŌņĀČ»Æļ¤¾§ĢåµÄĆܶČĪŖ£Ø””””£©
ČēĶ¼ŹĒĀČ»Æļ¤¾§ĢåµÄ¾§°ū½į¹¹Ź¾ŅāĶ¼£Ø¾§°ūŹĒÖø¾§ĢåÖŠ×īŠ”µÄÖŲø“µ„ŌŖ£©£¬ĘäÖŠŗŚĒņ±ķŹ¾ĀČĄė×Ó”¢°×Ēņ±ķŹ¾ļ¤Ąė×Ó£®ŅŃÖŖ¾§ĢåÖŠ2øö×ī½üµÄļ¤Ąė×ÓµÄŗĖ¼ä¾ąĄėĪŖa cm£¬ĀČ»Æļ¤µÄĦ¶ūÖŹĮæĪŖM g/mol£¬ŌņĀČ»Æļ¤¾§ĢåµÄĆܶČĪŖ£Ø””””£©| A£® | $\frac{2M}{{N}_{A}{a}^{3}}$g/cm3 | B£® | $\frac{M}{2{N}_{A}{a}^{3}}$g/cm3 | C£® | $\frac{M}{{N}_{A}{a}^{3}}$g/cm3 | D£® | $\frac{M{a}^{3}}{{N}_{A}}$g/cm3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | »ÆŗĻĪļ | B£® | Ńõ»ÆĪļ | C£® | ĪŽ»śĪļ | D£® | ¼ŲŃĪ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
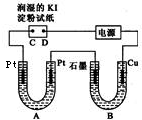 µē½ā×°ÖĆČēĶ¼ĖłŹ¾£¬Ķ¼ÖŠB×°ÖĆŹ¢ÓŠ1L2mol•L-1µÄNa2SO4ČÜŅŗ£¬A×°ÖĆŹ¢ÓŠ1L2mol•L-1µÄAgNO3ČÜŅŗ£¬Ķصēŗó£¬ŹŖČóµÄµķ·ŪKIŹŌÖ½µÄC¶Ė±äĄ¶É«£¬µē½āŅ»¶ĪŹ±¼äŗó£¬ŹŌ»Ų“š£ŗ
µē½ā×°ÖĆČēĶ¼ĖłŹ¾£¬Ķ¼ÖŠB×°ÖĆŹ¢ÓŠ1L2mol•L-1µÄNa2SO4ČÜŅŗ£¬A×°ÖĆŹ¢ÓŠ1L2mol•L-1µÄAgNO3ČÜŅŗ£¬Ķصēŗó£¬ŹŖČóµÄµķ·ŪKIŹŌÖ½µÄC¶Ė±äĄ¶É«£¬µē½āŅ»¶ĪŹ±¼äŗó£¬ŹŌ»Ų“š£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NO2 | B£® | NO | C£® | H2 | D£® | Cl2 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com