


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.消除硝酸工业尾气的污染 NO+NO2+2NaOH  2NaNO2+H2O 2NaNO2+H2O |
| B.工业上制CuSO4 2Cu+O2 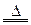 2CuO CuO+H2SO4 2CuO CuO+H2SO4 CuSO4+H2O CuSO4+H2O |
| C.乙炔水化法制乙醛 CH 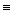 CH+H2O CH+H2O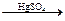 CH3CHO CH3CHO |
| D.消除硫酸厂尾气 |
 (NH4)2SO3
(NH4)2SO3查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.雨水样品酸度逐渐减小 |
| B.雨水样品酸度没有变化 |
| C.雨水样品继续吸收空气中的CO2 |
| D.雨水样品中的H2SO3被氧化成H2SO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
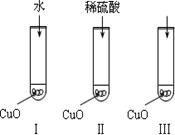
 (1)某同学提出的假设是 ;
(1)某同学提出的假设是 ; (2)通过实验Ⅰ可以证明 ;
(2)通过实验Ⅰ可以证明 ; (3)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅱ中加入稀硫酸后氧化铜溶解,则进一步所做的确认为:在Ⅲ中先加入 ,再加入 。
(3)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅱ中加入稀硫酸后氧化铜溶解,则进一步所做的确认为:在Ⅲ中先加入 ,再加入 。 (4)探究结果为 。
(4)探究结果为 。 (5)你认为除实验Ⅱ和Ⅲ所用的试剂外,还能溶解氧化铜的一种常见物质是 。
(5)你认为除实验Ⅱ和Ⅲ所用的试剂外,还能溶解氧化铜的一种常见物质是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.通过澄清石灰水 | B.先通过足量小苏打溶液,再通过石灰水 | C.先通过足量酸性高锰酸钾溶液,再通过澄清石灰水 | D.通过品红溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.SO2和Cl2的漂白原理相同 |
| B.SO3具有氧化性 |
| C.常温下,浓硫酸不与铜反应,是因为铜被钝化 |
| D.可用铁罐来进行贮存、运输冷的浓硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com