
在固态金属氧化物电解池中,高温共电解H2O—CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示。下列说法不正确的是( )
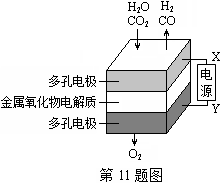 A.X是电源的负极
A.X是电源的负极
B.阴极的反应式是:H2O+2eˉ=H2+O2ˉ
CO2+2eˉ=CO+O2ˉ
C.总反应可表示为:H2O+CO2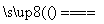 H2+CO+O2
H2+CO+O2
D.阴、阳两极生成的气体的物质的量之比是1︰1
科目:高中化学 来源: 题型:
欲从苯酚的乙醇溶液中分离苯酚和乙醇,有下列操作:①蒸馏 ②过滤 ③静置分液 ④加入足量的金属钠 ⑤通入过量的二氧化碳 ⑥加入足量的NaOH溶液 ⑦加入足量的FeCl3 溶液 ⑧加入乙酸与浓硫酸混合液加热。合理的实验操作步骤及顺序是( )
A、④⑤③ B、⑥①⑤③ C、⑧①⑦ D、⑧②⑤③
查看答案和解析>>
科目:高中化学 来源: 题型:
生活中遇到的某些问题,常常涉及到化学知识,下列各项叙述不正确的是( )
A.鱼虾放置时间过久,会产生腥臭味,应当用水冲洗,并在烹调时加入少量食醋
B.“酸可以除锈”,“洗涤剂可以去油”都是发生了化学变化
C.被蜂蚁蜇咬会感觉疼痛难忍,这是由于人的皮肤被注入了甲酸的缘故,此时若能涂抹稀氨水或碳酸氢钠溶液,可以减轻疼痛
D.苯酚可用做杀菌消毒剂,医用酒精可用于皮肤消毒,其原因均在于可使蛋白质变性凝固
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料。下列说法正确的是( )
A.元素A、B组成的化合物常温下一定呈气态
B.工业上常用电解法制备元素C、D、E的单质
C.化合物AE、CE都是电解质,融化状态下能被电解
D.一定条件下,元素D、E的最高价氧化物对应的水化物之间不能发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
⑴在一定的温度下,把2体积N2和6体积H2分别通入一个带活塞的体积可变的容器中,活塞的一端与大气相通容器中发生如下反应:N2(g)+3H2(g) 2NH3(g) △H<0。反应达到平衡后,测得混合气体为7体积。
2NH3(g) △H<0。反应达到平衡后,测得混合气体为7体积。
 (1)保持上述反应温度不变,设a、b、c分别表示加入的N2、H2 和NH3的体积,如果反应达到平衡后混合气体中各物质的量仍与上述平衡时完全相同。若需规定起始时反应向逆方向进行,则c的取值范围是 。
(1)保持上述反应温度不变,设a、b、c分别表示加入的N2、H2 和NH3的体积,如果反应达到平衡后混合气体中各物质的量仍与上述平衡时完全相同。若需规定起始时反应向逆方向进行,则c的取值范围是 。
⑵尿素CO(NH2)2是一种高效化肥,也是一种化工原料。密闭容器中以等物质的量NH3和CO2为原料,在1200C催化剂作用下反应生成尿素:
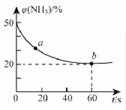
2NH3(g) + CO2(g)  CO(NH2)2 (s)+H2O(g)。混合气体中NH3的物质的量百分含量φ(NH3)随时间变化关系如右图所示。
CO(NH2)2 (s)+H2O(g)。混合气体中NH3的物质的量百分含量φ(NH3)随时间变化关系如右图所示。
则a点的正反应速率v正(CO2) b点的逆反应速率v逆(CO2)(填>、<或=); 氨气的平衡转化率是 。
⑶NH3催化氧化可得到的NO、NO2会污染环境。用间接电化学法除去NO的过程,如下图所示:
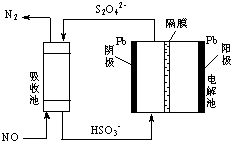
已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式: 。
用离子方程式表示吸收池中除去NO的原理: 。
⑷NO2会污染环境,可用Na2CO3溶液吸收NO2并生成CO2。已知9.2g NO2和Na2CO3溶液完全反应时转移电子0.1 mol,此反应的离子方程式是 ;
恰好反应后,使溶液中的CO2完全逸出,所得溶呈弱碱性,则溶液中离子浓度大小关系是c(Na+)> 。
查看答案和解析>>
科目:高中化学 来源: 题型:
一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是( )
A.反应CH4+H2O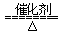 3H2+CO,每消耗1molCH4转移12mol 电子
3H2+CO,每消耗1molCH4转移12mol 电子
 B.电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
B.电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
C.电池工作时,CO32-向电极B移动
D.电极B上发生的电极反应为:O2+2CO2+4e-=2CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH可由电解法制备,钴氧化物可通过处理钴渣获得。
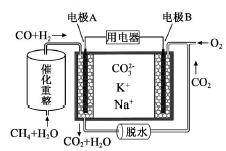
(1)利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。B极区电解液为__________溶液(填化学式),阳极电极反应式为__________ ,电解过程中Li+向_____电极迁移(填“A”或“B”)。
(2)利用钴渣[含Co(OH)3、Fe(OH)3等]制备钴氧化物的工艺流程如下:
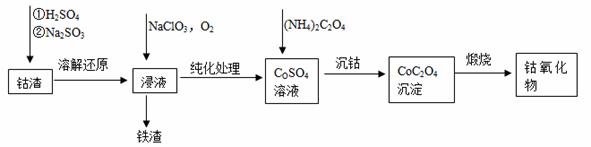
Co(OH)3溶解还原反应的离子方程式为____________________________________,铁渣中铁元素的化合价为___________,在空气中煅烧CoC2O4生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),则钴氧化物的化学式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ----------------------------------------------------( )
A.含有羟基的化合物一定属于醇类
B.代表醇类的官能团是跟链烃基相连的羟基
C.醇类和酚类具有相同的官能团,因而具有相同的化学性质
D.分子内有苯环和羟基的化合物一定是酚类
查看答案和解析>>
科目:高中化学 来源: 题型:
中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用。若1 mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为 ----------------------------------------------------------- -------------------------( )
-------------------------( )
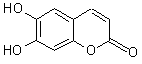 A 2 mol Br2 2 mol NaOH
A 2 mol Br2 2 mol NaOH
B 2 mol Br2 3 mol NaOH
C 3 mol Br2 4 mol NaOH
D 4 mol Br2 4 mol NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com