
【题目】根据以下背景资料,回答下列问题:
Ⅰ、不锈钢以其优异的抗腐蚀性能越来越受到人们的靑睐,它主要是由铁、铬、镍、铜、碳等元索所组成的合金。
Ⅱ、锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。
Ⅲ、砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。
Ⅳ、K2Cr2O7曾用于检测司机是否酒后驾驶:
Cr2O72-(橙色)+CH3CH2OH![]() Cr3+(绿色)+CH3COOH (未配平)
Cr3+(绿色)+CH3COOH (未配平)
(1)镍元素基态原子的电子排布式为_________________。
(2)CH3COOH分子中所含元素的电负性由大到小的顺序为___________,碳原子的轨道杂化类型为_________,所含σ键与π键的数目之比为______________________。
(3)AsCl3分子的立体构型为_____________,铁原子中有_________个未成对电子。
(4)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液,在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为______,提供孤电子对的原子是_____。
(5)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因____________________。
GeCl4 | GeBr4 | GeI4 | |
熔点/℃ | 49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
(6)某镍白铜合金的立方晶胞结构如图所示。
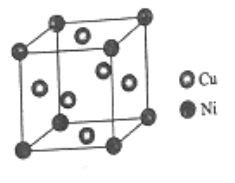
①晶胞中铜原子与镍原子的数量比为_____。
②若合金的密度为dg/cm3,晶胞参数a=________nm
【答案】1s22s22p63s23p63d84s2或【Ar】3d84s2O>C>Hsp3和sp27:1三角锥形4配位键NGeCl4、GeBr4、GeI4熔沸点依次升高;原因是分子结构相似,相对分子质量依次增大,分子间相互作用力逐渐增强3:1![]()
【解析】
(1)Ni是28号元素,其原子核外有28个电子,根据构造原理书写镍元素基态原子的电子排布式;3d能级上的未成对的电子数为2。(2)非金属性越强,电负性越强;乙酸分子中含有甲基碳原子和羧基碳原子,根据价层电子对互斥理论判断碳原子的轨道杂化类型;乙酸分子中单键为σ键,双键中含有1个σ键和1个π键,据此进行解答;(3)锗的卤化物都是分子晶体,相对分子质量越大,分子间作用力越强,熔沸点越高;(4)①该晶胞中Ni原子个数=8×1818=1、Cu原子个数=6×1212=3;②该晶胞的化学式为Cu3Ni,若合金的密度为dg/cm3,晶胞参数=![]() 。
。
(1)Ni是28号元素,其原子核外有28个电子,根据构造原理书写镍元素基态原子的电子排布式为1s22s22p63s23p63d84s2或[Ar]3d84s2;(2)CH3COOH分子中含有C、O、H元素,非金属性:O>C>H,则电负性:O>C>H;CH3COOH分子内含有甲基碳原子和羧基碳原子,甲基碳原子中形成4个σ键,为sp3杂化,羧基碳原子形成3个σ键,无孤对电子,杂化方式为sp2杂化;CH3COOH分子中含有3个C-H键、1个C-C键、1个O-H键、1个C-O单键及1个碳氧双键,单键为σ键,双键中含有1个σ键和1个π键,所以CH3COOH分子中含有7个σ键、1个π键,σ键与π键数目之比为7:1;(3)锗的卤化物都是分子晶体,分子间通过分子间作用力结合,对于组成与结构相似的分子晶体,相对分子质量越大,分子间作用力越强,熔沸点越高,由于相对分子质量:GeCl4<GeBr4<GeI4,故沸点:GeCl4<GeBr4<GeI4;(4)①该晶胞中Ni原子个数=8×![]() =1、Cu原子个数=6×
=1、Cu原子个数=6×![]() =3,则Cu、Ni原子个数之比为3:1;②该晶胞的化学式为Cu3Ni,若合金的密度为dg/cm3,晶胞参数=
=3,则Cu、Ni原子个数之比为3:1;②该晶胞的化学式为Cu3Ni,若合金的密度为dg/cm3,晶胞参数=![]() 。
。


科目:高中化学 来源: 题型:
【题目】用25mL18.4mol/L的浓硫酸与铜共热一段时间后,冷却,过滤除去多余的铜,将滤液稀释到100 mL,所得溶液中SO42-浓度为3mol/L,则此时溶液中CuSO4的物质的量浓度为
A. 0.5mol/L B. 1.6 mol/L C. 1.8 mol/L D. 3mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空。
I.现有下列10种物质①熔融的氢氧化钠 ②蔗糖 ③纯净的盐酸 ④金属钠 ⑤硫酸 ⑥二氧化硫 ⑦硫粉 ⑧石膏(CaSO4·2 H2O) ⑨酒精溶液 ⑩液氨
(1)属于电解质的有_____________________。
(2)属于非电解质的有_____。
(3)上述状态下能导电的有_____。
(4)上述状态下的电解质不能导电的有_____。
II.Fe(OH)2长时间露置于空气中发生变化的化学方程式为:___________________________。
偏铝酸钠溶液中通入足量二氧化碳反应的离子方程式为:____________________________。
III.高纯度单晶硅可以按下列方法制备:
![]()
写出步骤①的化学方程式________________________。
步骤②的产物经过冷凝后得到的SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点57.6℃),提纯SiHCl3主要操作的名称是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示的反应关系中,部分产物被略去。已知2 mol白色固体粉末X受热分解,恢复到室温生成白色固体A、无色液体B和无色气体C各1 mol。X、E、G的焰色反应均为黄色。

回答下列问题:
(1)写出下列物质的化学式:G_____________ D_____________
(2)写出G与C反应生成D的化学反应方程式:____________________________
(3)写出X+E→A的离子方程式:______________________________________
(4)写出C与Na2O2反应的化学方程式:_____________________________,若有0.2 mol Na2O2参加反应则转移的电子数目为_____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验仪器,用下图中的实验装置进行实验,证明过氧化钠可作供氧剂。

(1)A是制取CO2的装置,写出A中发生反应的离子方程式______________。
(2)填写表中空格:
仪器 | 加入试剂 | 加入该试剂的目的 |
B | 饱和NaHCO3溶液 | _____________ |
C | ___________ | _______________ |
D | NaOH溶液 | _____________ |
(3)写出过氧化钠与二氧化碳反应的化学方程式______________________。
(4)用_______________检验F中收集到的气体,现象是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有以下有机物:① ![]() ②
② ![]() ③
③ ![]() ④
④ ![]() ⑤苯酚
⑤苯酚
(1)能与Na反应的是 ________ ;
(2)能与![]() 溶液反应的有_________;
溶液反应的有_________;
(3)能与NaHCO3溶液反应有气泡产生的是_______________;
(4)能与银氨溶液发生银镜反应的有____________________;
(5)既能发生消去反应,又能发生酯化反应的有___________________;
(6)能发生氧化反应的有(除燃烧以外)___________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20℃时,NaCl溶解于水的实验数据如下表所示
实验序号 | 水的质量/g | 加入的NaCl质量/g | 未溶的NaCl质量/g |
10 | 2 | 0 | |
10 | 3 | 0 | |
10 | 4 | 0.4 |
下列叙述正确的是( )
A. 实验①所得的溶液为饱和溶液 B. 实验②所得的溶液为饱和溶液
C. 20℃时NaCl的溶解度为30g D. 实验①所得溶液的溶质质量分数为16.7%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)加热13.7g Na2CO3和NaHCO3的混合物至质量不再变化,恢复至室温,剩余固体的质量为10.6g,则混合物中NaHCO3的物质的量为___________。
(2)根据反应8NH3 + 3Cl2=N2+ 6NH4Cl,回答下列问题:
①该反应中______元素被还原,______元素被氧化;
②在该反应中,若有0.3mol电子发生转移,在标准状况下,可生成N2的体积为______L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com