
废电池造成污染的问题日益受到关注。下列有关电池的说法正确的是
A. 构成原电池的正极和负极必须是两种不同的金属
B. 弱电解质在水中的电离程度报小,不能用作电池的电解质溶液
C. 原电池是将化学能完全转变为电能的装置
D. 回收废旧电池,可防止汞、镉和铅等重金属对土壤和水源的污染
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源:2016-2017学年山东省高二下学期开学考试化学试卷(解析版) 题型:选择题
汽车尾气中,产生NO的反应为:N2(g)+O2(g) 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。下列叙述正确的是
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。下列叙述正确的是
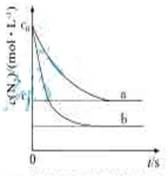
A. 温度T下,该反应的平衡常数K=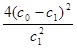
B. 温度T下,随着反应的进行,混合气体的密度减小
C. 曲线b对应的条件改变可能是加入了催化剂
D. 若曲线b对应的条件改变是温度,可判断该反应的△H<0
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上学期期末考试理综化学试卷(解析版) 题型:推断题
高分子树脂M具有较好的吸水性,其合成路线如下:
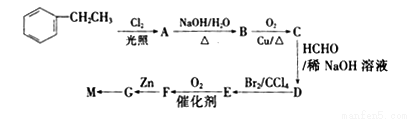
已知: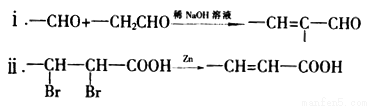
(1)C的名称为______________,D中的官能团为__________________,结构简式为_____________。
(2)由A生成B的化学方程式为___________________。
(3)上述合成路线中,D→E转化在合成M中的作用为___________________________。
(4)下列关于F的叙述正确的是___________。
A.能与NaHCO3反应生成CO2 B.能发生水解反应和消去反应
C.能聚合成高分子化合物 D. 1 mol G最多消耗2 mol NaOH
(5)H是G的同系物,且与G相差一个碳原子,则同时满足下列条件的H的同分异构体共有______种(不考虑立体异构)。
①与G具有相同的官能团 ②苯环上只有两个取代基
(6)根据上述合成路线和信息,以苯乙醛为原料(其他无机试剂任选),设计制备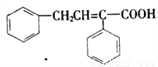 的合成路线_________________________。
的合成路线_________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省天水市高二下学期开学考试(寒假作业检测)化学试卷(解析版) 题型:选择题
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
A. 0.1 mol•L﹣1CH3COONa溶液与0.1 mol•L﹣1HCl溶液等体积混合:c(Na+)=c(Cl﹣)>c(CH3COO﹣)>c(H+)
B. 0.1 mol•L﹣1NH4Cl溶液与0.1 mol•L﹣1氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl﹣)>c(OH﹣)
C. 0.1 mol•L﹣1Na2CO3溶液与0.1 mol•L﹣1NaHCO3溶液等体积混合:2/3 c(Na+)=c(CO32﹣)+c(HCO3﹣)+c(H2CO3)
D. 0.1 mol•L﹣1Na2C2O4溶液与0.1 mol•L﹣1HCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42﹣)+c(HC2O4﹣)+c(OH﹣)=c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省天水市高二下学期开学考试(寒假作业检测)化学试卷(解析版) 题型:选择题
下列说法正确的是
A. H2(g)的燃烧热△H=-285.8 kJ/mol,则2H2O(g)=2H2(g)+O2(g) △H=+571.6 kJ/mol
B. 反应物的总能量低于生成物的总能量时,该反应为放热反应
C. 由石墨比金刚石稳定可知:c(金刚石,s)=c(石墨,s) △H<0
D. 已知:298K时,N2(g)+3H2(g)  2NH3(g) △H=-92.0 kJ/mol。在相同温度下,向密闭容器中通入0.5 mol N2和1.5mol H2,达到平衡时放出46.0 kJ的热量
2NH3(g) △H=-92.0 kJ/mol。在相同温度下,向密闭容器中通入0.5 mol N2和1.5mol H2,达到平衡时放出46.0 kJ的热量
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省景德镇市高二(素质班)上学期期末考试化学试卷(解析版) 题型:推断题
Ⅰ.已知A、B、C为中学化学中常见的单质。室温下,A为固体,B和C均为气体。在适宜的条件下,它们可以按如下框图进行反应。
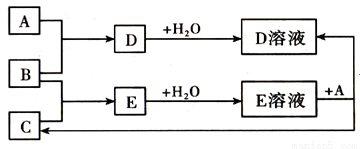
回答下列问题:
组成单质A、B、C的三种元素中的任意两种元素形成的化合物所属物质类别一定不是_____________。
①氢化物 ②酸 ③碱 ④盐 ⑤氧化物
如果E溶液是一种强酸,则E的化学式为_________________。
Ⅱ.下图是一些常见元素的单质或化合物之间的转化关系。溶液中的水以及部分反应物或生成物未标出。A、E是空气中的两种主要成分,C是由两种元素组成的新型材料,并且C的原子数、最外层电子数之和与SiC相同,J是一种能引起温室效应的气体,K是两性化合物。反应③、④、⑤用于工业中生产H。
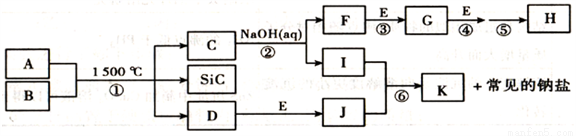
回答下列问题:
写出A的电子式:________________,G的化学式:________________;
写出D和H反应的化学方程式:_____________________________________________;
写出反应⑥的离子方程式:_________________________________________;
B和SiC的纳米级复合粉末是新一代大规模集成电路理想的散热材料。反应①是科学家研究开发制备该纳米级复合粉末的最新途径。已知B由Si及另外两种元素组成,且Si与另外两种元素的物质的量之比均为1:4,写出反应①的化学方程式:____________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省景德镇市高二(素质班)上学期期末考试化学试卷(解析版) 题型:选择题
根据键能数据估算CH4(g)+4F2(g)═CF4(g)+4HF(g)的反应热△H为( )
化学键 | C—H | C—F | H—F | F—F |
键能/(kJ | 414 | 489 | 565 | 155 |
A. -485 kJ mol-1 B. +485 kJ
mol-1 B. +485 kJ mol-1 C. +1940 kJ
mol-1 C. +1940 kJ mol-1 D. -1940 kJ
mol-1 D. -1940 kJ mol-1
mol-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省庄河市高一上学期期末考试化学试卷(解析版) 题型:选择题
化学反应3Fe2++2S2O32-+O2+aOH-=Fe3O4+S4O62-+2H2O是水热法制备Fe3O4纳米颗粒的原理。下列说法正确的是( )
A. 参加反应的Fe2+全部作还原剂
B. 生成1.5molFe3O4时,反应转移电子 6mol电子
C. 方程式中a=2
D. 反应中被氧化的元素是Fe,被还原的元素是S和O
查看答案和解析>>
科目:高中化学 来源:2017届山东省淄博市高三第一次模拟考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 18g重水(D2O)所含的电子数为10NA
B. 常温常压下,0.3molNO2完全与水反应,转移的电子数为0.2NA
C. 标准状况下,22.4LCCl4中含有NA个CCl4分子
D. 常温下, 1L0.1mol/LCH3COONH4溶液中NH4+离子数为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com