
分析 ①NaCl 属于强酸强碱盐溶液显中性,
②NH4Cl 是强酸弱碱盐,溶液中铵根离子水解溶液显酸性,
③Na2CO3是强碱弱酸盐,溶液中碳酸根离子水解溶液显碱性,
④CH3COONa 是强碱弱酸盐,溶液中醋酸根离子水解溶液显碱性,
⑥NaHCO3 是强碱弱酸盐,溶液中碳酸氢根离子水解溶液显碱性,
⑦Cu(NO3)2 属于强酸弱碱盐,铜离子水解溶液显酸性,
⑧CH3COONH4 是弱酸弱碱盐,铵根离子和醋酸根离子水解程度相当溶液呈中性,
⑨FeCl3是强酸弱碱盐,溶液中铁离子水解溶液显酸性,
⑩Na2S是强碱弱酸盐,溶液中硫离子水解溶液显碱性.
解答 解:①NaCl 属于强酸强碱盐溶液显中性,
②NH4Cl 是强酸弱碱盐,溶液中铵根离子水解溶液显酸性,
③Na2CO3是强碱弱酸盐,溶液中碳酸根离子水解溶液显碱性,
④CH3COONa 是强碱弱酸盐,溶液中醋酸根离子水解溶液显碱性,
⑥NaHCO3 是强碱弱酸盐,溶液中碳酸氢根离子水解溶液显碱性,
⑦Cu(NO3)2 属于强酸弱碱盐,铜离子水解溶液显酸性,
⑧CH3COONH4 是弱酸弱碱盐,铵根离子和醋酸根离子水解程度相当溶液呈中性,
⑨FeCl3是强酸弱碱盐,溶液中铁离子水解溶液显酸性,
⑩Na2S是强碱弱酸盐,溶液中硫离子水解溶液显碱性;
(1)上述分析可知溶液呈酸性的有②⑦⑨,溶液呈碱性的有③④⑤⑩,呈中性的有①⑧,
故答案为:②⑦⑨;③④⑤⑩;①⑧;
(2)②NH4Cl 是强酸弱碱盐,溶液中铵根离子水解溶液显酸性,水解离子方程式为:NH4++H2O?NH3•H2O+H+,
③Na2CO3是强碱弱酸盐,溶液中碳酸根离子水解溶液显碱性,水解离子方程式为:CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-,
⑨FeCl3是强酸弱碱盐,溶液中铁离子水解溶液显酸性,Fe3++3H2O?Fe(OH)3+3H+,
故答案为:NH4++H2O?NH3•H2O+H+;CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-;Fe3++3H2O?Fe(OH)3+3H+.
点评 本题考查了盐类水解的分析判断,主要是溶液酸碱性的判断和离子方程式的书写,题目难度不大.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④ | C. | ①④ | D. | ① |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 、
、 CH3CH═CHCHO+H2O
CH3CH═CHCHO+H2O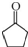 ,D中官能团的名称为碳碳双键、氯原子.
,D中官能团的名称为碳碳双键、氯原子. .
.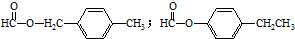 .
. )的合成路线:CH3CH2CH2CH2OH$→_{△}^{浓硫酸}$CH3CH2CH=CH2$\stackrel{NBS}{→}$CH3CHBrCH=CH2$→_{△}^{NaOH醇溶液}$CH2=CHCH=CH2$\stackrel{一定条件}{→}$
)的合成路线:CH3CH2CH2CH2OH$→_{△}^{浓硫酸}$CH3CH2CH=CH2$\stackrel{NBS}{→}$CH3CHBrCH=CH2$→_{△}^{NaOH醇溶液}$CH2=CHCH=CH2$\stackrel{一定条件}{→}$ .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖能发生酯化反应 | |
| B. | 葡萄糖具有还原性 | |
| C. | 葡萄糖充分燃烧的产物为CO2与H2O | |
| D. | 完全燃烧等质量的葡萄糖和甲醛,所需氧气物质的量不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子最外层电子数小于4的元素一定为金属元素 | |
| B. | 质子数等于电子数的某微粒,可能是一种分子或一种原子 | |
| C. | 第ⅠA族元素的金属性一定比第ⅡA族元素的金属性强 | |
| D. | 非金属元素形成的化合物只有共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 元素 性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
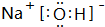 ; 属离子化合物(填“离子”或“共价”).
; 属离子化合物(填“离子”或“共价”). 查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三个烧杯中均会发生的离子反应为2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 三个烧杯中钠均在液面上剧烈反应,且X烧杯中反应最剧烈 | |
| C. | 三个烧杯反应后,生成的溶质的物质的量浓度相同 | |
| D. | 三个烧杯反应后,生成的气体的质量一定相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com