
【题目】常温下,可逆反应2NO2![]() 2NO+O2在恒容密闭容器中进行,达到平衡状态的标志是
2NO+O2在恒容密闭容器中进行,达到平衡状态的标志是
①单位时间内生成nmolO2的同时生成2nmolNO2;
②单位时间内生成nmolO2的同时生成2nmolNO;
③混合气体的密度不再改变;
④混合气体的颜色不再改变;
⑤密闭容器中压强不再改变;
A.②③⑤B.①③⑤C.①④⑤D.全部
【答案】C
【解析】
①单位时间内生成nmolO2的同时生成2nmolNO2,则v正=v逆,已达平衡,①正确;
②单位时间内生成nmolO2的同时生成2nmolNO,描述的都是正反应,不能说明已达平衡,②错误;
③该反应气体的总质量、体积永远不变,故混合气体的密度永远不变,即混合气体的密度不再改变不能说明反应是否平衡,③错误;
④若该反应还未平衡,则红棕色的NO2的浓度改变,气体的颜色必然改变,当混合气体的颜色不再改变,说明反应已达平衡,④正确;
⑤该反应的气体总物质的量改变,体积不变,正向进行压强增大;密闭容器中压强不再改变,说明反应是否平衡,⑤正确;
综上所述,①④⑤是该可逆反应达到平衡状态的标志。
答案选C。


科目:高中化学 来源: 题型:
【题目】(1)画出下列各微粒的结构示意图:L层电子数为K、M层电子数之和的原子形成的阴离子________;与Ne原子电子层结构相同的+1价阳离子________。
(2)写出下列物质或离子的电子式
N2 ________CO2 _________ OH- ____________NH![]() ___________
___________
(3)用电子式表示H2S和MgBr2的形成过程
H2S ________________________________
MgF2_______________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100mL混合溶液中,H2SO4和HNO3的物质的量浓度分别是4.0mol/L和2.0mol/L,向该混合溶液中加入25.6g铜粉,加热,待充分反应后,静置,得到蓝色澄清溶液(假设反应后溶液体积不变)。下列说法中正确的是( )
A.产生的NO在标准状况下的体积是1.12L
B.反应后溶液中Cu2+的物质的量浓度为3.0mol/L
C.反应后溶液中H+的物质的量浓度为8.0mol/L
D.在反应后的溶液中加0.6molNaOH刚好使Cu2+完全沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖颁给了三位为锂离子电池发展作出重要贡献的科学家。磷酸铁锂锂离子电池充电时阳极反应式为:LiFePO4 -xLi+ -xe-→ xFePO4 +(1-x)LiFePO4。放电工作示意图如图。下列叙述不正确的是
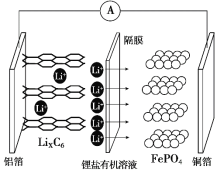
A.放电时,Li+通过隔膜移向正极
B.放电时,电子由铝箔沿导线流向铜箔
C.放电时正极反应为:FePO4+xLi+ +xe-→xLiFePO4 +(1-x)FePO4
D.磷酸铁锂锂离子电池充放电过程通过Li+迁移实现,C、Fe、P元素化合价均不发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将2molSO2和1molO2充入一定容积的密闭容器中,在催化剂作用下发生如下反应:2SO2(g)+O2(g)![]() 2SO3(g)ΔH=-197kJ·mol-1,当达到化学平衡时,下列说法中正确的是
2SO3(g)ΔH=-197kJ·mol-1,当达到化学平衡时,下列说法中正确的是
A.v正(O2)=2v逆(SO2)B.SO2和SO3共2mol
C.放出197kJ热量D.SO2和O2浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
Ⅰ.如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图(图中涉及物质均为气态),请写出NO2和CO反应的热化学方程式:______
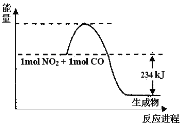
Ⅱ.现有①BaCl2②水晶③金属铝④Na2SO4⑤冰⑥碘片六种物质,按下列要求回答(填编号,下同):
(1)熔化时不需要破坏化学键的是_______,熔化时需要破坏共价键的是_______,能导电的是______。
(2)属于离子化合物的是________,只有离子键的物质是________,属于共价化合物的是______。
(3)①的电子式是________;⑤的结构式是________,⑤的空间构型是______,⑤中分子间作用力除了范德华力外,还含有______,因此而引起一些特殊的性质,请举出一种:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“氮的固定”对保障人类生存具有重大意义。一种新型合成氨的原理如图所示:
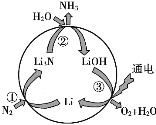
(1)N2的电子式:_____。
(2)Li3N中含有的化学键类型是_____。
(3)热稳定性:NH3_____H2O(填“>”或“<”)。
(4)NH3 、H2O分子中化学键极性更强的是_____,从原子结构角度解释原因:_____。
(5)写出右图所示过程的总反应方程式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分离和提纯是化学研究物质的基本方法。请选择分离提纯下列物质所用的装置(填字母序号):
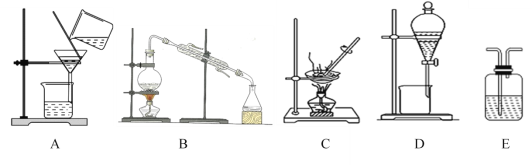
(1)除去粗食盐水中的泥沙___;
(2)用CCl4萃取碘水中的碘___;
(3)用自来水制取蒸馏水___;
(4)用酸性KMnO4溶液除去CO2中的SO2___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g) + 6H2O(g),下列叙述正确的是
4NO(g) + 6H2O(g),下列叙述正确的是
A.平衡时,v正(O2)=v逆(O2)必成立
B.关系式5v正(O2)=4v正(NO)总成立
C.用上述四种物质NH3、O2、NO、H2O表示的正反应速率的数值中,v正(H2O)最小
D.若投入4 mol NH3和5 mol O2,通过控制外界条件,必能生成4 mol NO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com