
| A. | 常温下向饱和AgCl水溶液中加入盐酸,Ksp值变大 | |
| B. | 在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 | |
| C. | 用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小 | |
| D. | 物质的溶解度随温度的升高而增加,物质的溶解都是吸热的 |
分析 A.Ksp值只与温度有关;
B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,Ksp值不变,结合Ksp判断;
C.AgCl溶液中存在:AgCl(s)?Ag+(aq)+Cl-(aq),从平衡移动的角度分析;
D.物质的溶解度不一定随温度的升高而增大,如氢氧化钙溶液随温度的升高溶解度减小.
解答 解:A.Ksp值只与温度有关,向饱和AgCl水溶液中加入盐酸,由于温度不变,所以Ksp值不变,故A错误;
B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(SO4)增大,Ksp值不变,故(Ba2+)减小,故B错误;
C.AgCl溶液中存在:AgCl(s)?Ag+(aq)+Cl-(aq),Cl-浓度越大,则溶解的AgCl越少,所以用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小,故C正确;
D.物质的溶解度不一定随温度的升高而增大,如氢氧化钙溶液随温度的升高溶解度减小,故D错误.
故选C.
点评 本题考查难溶电解质的溶解平衡,为高频考点,侧重于学生的分析能力的考查,注意把握难溶电解质的溶解平衡的影响因素,难度不大.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
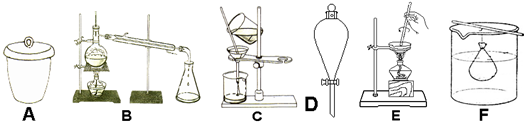
| A. | 中和滴定实验时,用待测液润洗锥形瓶 | |
| B. | 盛放Na2SiO3溶液时,使用带玻璃塞的磨口瓶 | |
| C. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| D. | NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 晶体 | NaCl | MgO | AlBr3 | SiCl4 | 共价化合物R |
| 熔点(℃) | 801 | 2852 | 97.5 | -70 | 1723 |
| 沸点(℃) | 1413 | 3600 | 263.3 | 57 | 2230 |
| A. | SiCl4是分子晶体 | B. | MgO比NaCl的晶格能大 | ||
| C. | R是原子晶体 | D. | AlBr3为离子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁粉有剩余,溶液呈浅绿色,Cl-基本保持不变 | |
| B. | 往溶液中滴入无色KSCN溶液,溶液变红色 | |
| C. | Fe2+和Fe3+物质的量之比为5:1 | |
| D. | 氧化产物和还原产物的物质的量之比为2:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两元素形成的最高价氧化物水化物的酸性A强于B | |
| B. | A的气态氢化物比B的气态氢化物稳定 | |
| C. | A的金属性比B的金属性强 | |
| D. | A的阴离子比B的阴离子还原性弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Mg、Al的还原性依次增强 | |
| B. | HF、HCl、HBr的热稳定性依次增强 | |
| C. | H3PO4、H2SO4、HClO4的酸性依次增强 | |
| D. | LiOH、NaOH、KOH、CsOH的碱性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3熔点很高,工业上还可采用电解熔融AlCl3的方法冶炼Al | |
| B. | 灼烧某物质时,用眼直接观察到火焰呈黄色,则可判断该物质不含钾元素 | |
| C. | 向新制的FeSO4溶液中滴入适量的NaOH溶液,放置片刻,整个反应过程的颜色变化是:浅绿色溶液→白色沉淀→灰绿色沉淀→红褐色沉淀 | |
| D. | 称取等质量的两份铝粉,分别加入过量的稀HCl和过量的NaOH溶液中,则放出氢气的体积(同温同压下)不相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com