
A、B、C、D均为短周期元素,B、A可形成两种液态化合物,其原子个数比分别为1∶1和2∶1,且分子中电子总数分别为18和10。B与D能形成一种极易溶于水的碱性气体X,B与C能形成极易溶于水的酸性气体Y,Y分子中的电子数为18。A、B、D能形成一种离子化合物,其水溶液呈弱酸性。请写出:
(1)C的元素符号__________,X跟Y反应的化学方程式_____________________________。
(2)用离子方程式解释A、B、D形成的化合物水溶液呈弱酸性的原因是________________
_____________________________________________。
(3)铋(Bi)跟C元素能形成化合物BiCl3,其水解生成难溶于水的BiOCl。
①BiCl3水解反应的化学方程式为__________________________________________。
②把适量的BiCl3溶于含有少量Y的水中,能得到澄清溶液,试分析可能的原因。
③医药上把BiOCl叫做“次某酸铋”,分析这种叫法的不合理之处。
(1)Cl NH3+HCl====NH4Cl
(2)NH+4+H2O![]() NH3·H2O +H+
NH3·H2O +H+
(3)①BiCl3+H2O====BiOCl↓+2HCl
②盐酸能抑制BiCl3的水解。
③BiOCl中的Cl的化合价为-1。
(1)由题意知,A、B为H、O,B、D为N、H,故B为H,A为O,D为N,又B与C能形成极易溶于水的酸性气体Y,Y分子中的电子数为18,确定Y为HCl,故C为Cl。(2)NH4NO3为强酸弱碱盐,故水解显酸性。(3)化合物的命名有一定的规律和习惯。常见的有高、亚、次,原、正、偏。对于氯元素,只有+1价的才能叫“次某某”。故BiOCl叫做次氯酸铋不合理。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | |
| C | D |




查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D均为短周期元素,A和B是同周期相邻的两种元素,A和C是同主族相邻的两种元素:A、B、C三种元素的原子序数之和为31;D元素与A、B、C三种元素既不是同周期,也不同主族.请回答:
A、B、C、D均为短周期元素,A和B是同周期相邻的两种元素,A和C是同主族相邻的两种元素:A、B、C三种元素的原子序数之和为31;D元素与A、B、C三种元素既不是同周期,也不同主族.请回答:

 NH3?H2O+H+
NH3?H2O+H+ NH3?H2O+H+
NH3?H2O+H+ 2NH3
2NH3 2NH3
2NH3

| 4(m-n) |
| 5 |
| 4(m-n) |
| 5 |
| 4n+m |
| 5 |
| 4n+m |
| 5 |
| 4m+3n |
| 5 |
| 4m+3n |
| 5 |
| m-3n |
| 5 |
| m-3n |
| 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| △ |
| △ |
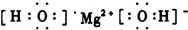
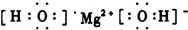
| △ |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
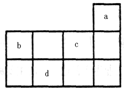 a、b、c、d均为短周期元素,它们在周期表中的位置如图所示.下列说法正确的是( )
a、b、c、d均为短周期元素,它们在周期表中的位置如图所示.下列说法正确的是( )| A、a原子的最外电子层上有8个电子 | B、c的最高价氧化物对应水化物为强酸 | C、d的原子半径比c的大 | D、b的非金属性比c的强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com