
| 实验 序号 | 反应温 度/℃ | Na2S2O3溶液 | 稀硫酸 | H2O | ||
| V/mL | c/mol•L-1 | V/mL | c/mol•L-1 | V/mL | ||
| ① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| ② | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
| ③ | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
分析 Ⅰ.(1)实验①、②的温度不同,故可探究温度对反应速率的影响,而要探究温度对反应速率的影响,则必须保持其他影响因素一致;
(2)A、在一张白纸上用黑墨水笔在白纸上画粗浅一致的“+”字做参照物,更有利于准确记录反应时间的长短;
B、该实验所需的计量仪器有量筒、温度计和秒表;
C.实验时,应先将量取的量取的Na2S2O3溶液置于相应温度的热水浴中后,然后迅速倒入H2SO4溶液,记录每组反应所需时间;
(3)二氧化硫易溶于水,1体积水能溶解40体积二氧化硫.
Ⅱ.(4)根据化学反应速率的公式V=$\frac{△c}{△t}$计算;
(5)由图象数据可以得出,用不同初始浓度,不同温度下的平均速率的大小来说明.
解答 解:Ⅰ.(1)实验①、②的温度不同,故可探究温度对反应速率的影响;而要探究温度对反应速率的影响,则必须保持其他影响因素一致:即加入的Na2S2O3溶液的量相同,故V1=10.0mL,加入的硫酸的量相同,故V2=10.0mL,加入水的体积相等,故V3=0,
故答案为:温度;10.0;10.0;0;
(2)A、在一张白纸上用黑墨水笔在白纸上画粗浅一致的“+”字做参照物,更有利于准确记录反应时间的长短,故A正确;
B、该实验需要量取溶液的体积、称量反应体系的温度和记录溶液变浑浊的时间,故所需的计量仪器有量筒、温度计和秒表,故B错误;
C.实验时,应先将量取的量取的Na2S2O3溶液置于相应温度的热水浴中后,然后迅速倒入H2SO4溶液,记录每组反应所需时间,而不能先混合后进行水浴加热,故C错误;
故答案为:A;
(3)二氧化硫易溶于水,1体积水能溶解40体积二氧化硫,故无法准确测量其体积,
故答案为:SO2易溶于水,无法准确测量其体积;
Ⅱ.(4)化学反应速率V=$\frac{△c}{△t}$=$\frac{2.2mol/L-1.9mol/L}{6min}$=0.05mol/(L•min),
故答案为:0.05mol/(L•min);
(5)因25℃反应物起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15℃大,
故答案为:25℃反应物起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15℃大.
点评 本题考查对影响反应速率的因素的探究实验,应注意的是在探究一个对反应速率的影响因素的时候,应保持其他的影响因素一致,注重了基础知识的考查,本题难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ${V}_{N{H}_{3}}$=0.6mol/L•min | B. | ${V}_{{N}_{2}}$=0.005mol/L•s | ||
| C. | ${V}_{{H}_{2}}$=0.9mol/L•min | D. | ${V}_{N{H}_{3}}$=0.02mol/L•s |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.
化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.| 实验序号 | 体积V/mL | 时间/s | |||
| Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
| ① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
| ② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
| ③ | 6.0 | 2.0 | 4.0 | Vx | t3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同温度下,CuS的溶解度小于ZnS的溶解度 | |
| B. | 除去工业废水中的Fe2+,可以选用CuS做沉淀剂 | |
| C. | 足量CuSO4溶解在0.1mol/L的H2S溶液中,Cu2+能达到的最大浓度为1.3×10-35mol/L | |
| D. | 在ZnS的饱和溶液中,加入FeCl2溶液,一定不产生FeS沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔点801℃,易溶于水 | B. | 熔点10.31℃,液态不导电 | ||
| C. | 熔点112.8℃,能溶于CS2 | D. | 熔点97.81℃,固态能导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
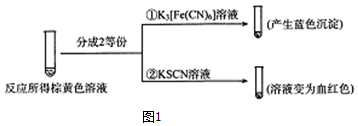
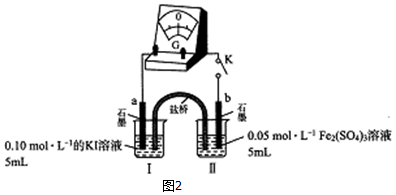
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用灼烧的方法可以区分羊毛和人造纤维 | |
| B. | 医用消毒酒精是体积分数为95%的乙醇 | |
| C. | 食用一定量的油脂能促进人体对某些维生素的吸收 | |
| D. | 加热能杀死流感病毒是因为蛋白质受热变性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com