
以下物质间的转化通过一步反应不能实现的是()
A. HCl→Cl2→HClO→NaClO B. Na→Na2O2→Na2CO3→NaHCO3
C. Si→SiO2→H2SiO3→Na2SiO3 D. Al→NaAlO2→Al(OH)3→Al2O3
考点: 硅和二氧化硅;氯、溴、碘及其化合物的综合应用;钠的重要化合物;镁、铝的重要化合物.
专题: 卤族元素;碳族元素.
分析: 根据各单质及其化合物的化学性质解答.
A、浓盐酸与强氧化剂如二氧化锰、高锰酸钾、氯酸钾等反应生成氯气,氯气与水反应生成次氯酸,次氯酸是弱酸,与碱反应生成盐;
B、钠在氧气中燃烧产物生成过氧化钠,过氧化钠和二氧化碳反应生成碳酸钠和氧气,碳酸钠可以与二氧化碳、水反应生成碳酸氢钠;
C、硅和氧气反应生成二氧化硅,属于酸性氧化物,但不与水反应,能和烧碱反应生成硅酸钠,再加入强酸可制得硅酸;
D、铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,偏铝酸钠与酸反应可以生成氢氧化铝,难溶性的碱受热易分解,分解为相应的氧化物与水.
解答: 解:A、浓盐酸与强氧化剂如二氧化锰、高锰酸钾、氯酸钾等反应生成氯气,氯气与水反应生成次氯酸,次氯酸是弱酸,与氢氧化钠反应生成次氯酸钠与水,故A正确;
B、钠在氧气中燃烧产物生成过氧化钠,过氧化钠和二氧化碳反应生成碳酸钠和氧气,碳酸钠可以与二氧化碳、水反应生成碳酸氢钠,故B正确;
C、硅和氧气反应生成二氧化硅,属于酸性氧化物,但不与水反应,SiO2不能一步生成H2SiO3,二氧化硅与烧碱反应生成硅酸钠,再加入强酸可制得硅酸,故C错误;
D、铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,偏铝酸钠与酸反应可以生成氢氧化铝,氢氧化铝加热分解生成氧化铝,故D正确.
故选C.
点评: 本题考查元素化合物物质之间的转化等,比较基础,掌握物质的性质是解答本题的关键,注意基础知识的积累掌握.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
氢气是一种新型的绿色能源,又是一种重要的化工原料.
合成氨反应的热化方程式如下:
N2(g)+3H2(g)⇌2NH3(g);△H=﹣92.4kJ/mol
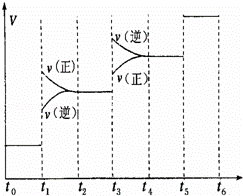
(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示.
图中t1时引起平衡移动的条件可能是 ,
其中表示平衡混合物中NH3的含量最高的一段时间是 ,若t0﹣t1,t1﹣t3,t3﹣t5这三段平衡常数分别用K1,K2,K3表示,那么K1,K2,K3的大小关系是
(2)若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”、“向右”或“不”);使用催化剂反应的△H (填“增大”、“减小”或“不改变”).
(3)温度为T℃时,将2a mol H2和 a mol N2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则反应的平衡常数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
从固体混合物A出发可以发生如下框图所示的一系列变化。
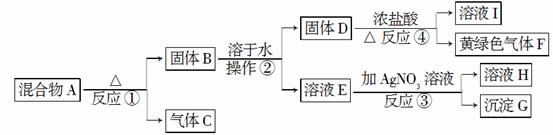
G为不溶于稀硝酸的白色固体;溶液H的焰色反应呈紫色(透过蓝色的钴玻璃观察)。回答下列问题:
(1)在实验室中收集气体C,可选择如图装置中的________。
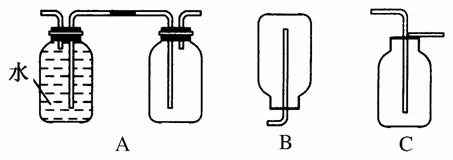
(2)操作②的名称是________。在操作②中所使用的玻璃仪器的名称是________。在得到固体D时必须进行洗涤、干燥等操作,洗涤固体D的目的是________________________________________。
(3)写出反应①的化学方程式、反应④的离子方程式:
反应①:_____________________________________________,
反应④:___________________________________________。
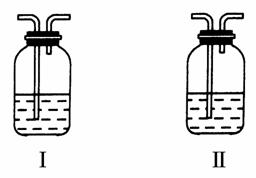
(4)在实验室中,要获得干燥纯净的黄绿色气体F,可以将它依次通过如图中的Ⅰ、Ⅱ装置,其中瓶Ⅰ中盛放的是________,瓶Ⅱ中盛放的是________。
(5)实验中必须吸收多余的气体F,以免污染空气。下图是实验室用NaOH溶液吸收气体F的装置,为防止产生倒吸现象,合理的装置是________。
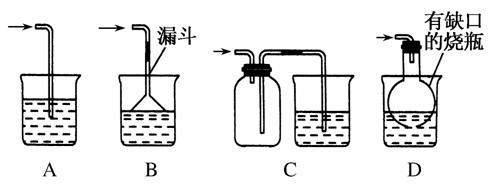
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学用语表示正确的是()
A. 氯化钙的电子式: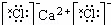
B. 168O2﹣离子的结构示意图: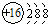
C. H2CO3的电离方程式:H2CO3⇌2H++CO32﹣
D. 葡萄糖的结构简式:C6H12O6
查看答案和解析>>
科目:高中化学 来源: 题型:
下列应用套管实验装置(部分装置未画出)进行的实验,叙述错误的是()
A. 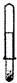
利用此装置可以制取少量H2
B. 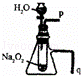
利用此装置可以验证Na2O2与水反应既生成氧气,又放出热量
C. 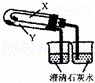
利用此装置验证KHCO3和K2CO3的热稳定性,X中应放的物质是K2CO3
D. 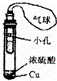
利用此装置制取SO2,并检验其还原性,小试管中的试剂可为酸性KMnO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
已知,将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3 ,且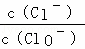 的值与温度高低有关,当n(KOH)=a mol时,下列有关说法错误的是()
的值与温度高低有关,当n(KOH)=a mol时,下列有关说法错误的是()
A. 若某温度下,反应后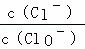 =11,则溶液中
=11,则溶液中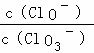 =
=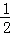
B. 参加反应的氯气的物质的量小于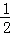 a mol
a mol
C. 改变温度,反应中转移电子的物质的量ne的范围: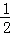 a mol≤ne≤
a mol≤ne≤ a mol
a mol
D. 改变温度,产物中KC1O3的最大理论产量为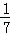 a mol
a mol
查看答案和解析>>
科目:高中化学 来源: 题型:
氮的重要化合物如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等,在生产、生活中具有重要作用.
(1)使用NaBH4为诱导剂,可使Co2+与肼在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体.
①写出该反应的离子方程式:.
②在纳米钴的催化作用下,肼可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝.若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如下图1所示,则N2H4发生分解反应的化学方程式为:;为抑制肼的分解,可采取的合理措施有(任写一种).
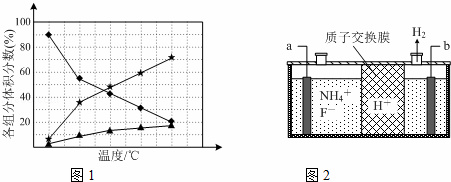
(2)在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如上图2所示.
①氮化硅的化学式为
②a电极为电解池的阳(填“阴”或“阳”)极,写出该电极的电极反应式:电解过程中还会生成少量氧化性极强的气体单质,该气体的分子式是F2.
查看答案和解析>>
科目:高中化学 来源: 题型:
元素R的最高价含氧酸的化学式为HnRO2n﹣2,则在气态氢化物中R元素的化合价为()
A. 12﹣3n B. 3n﹣12 C. 3n﹣10 D. 6﹣3n
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com