
| A、天平左盘放砝码,右盘放固体 |
| B、容量瓶使用时含有少量的蒸馏水 |
| C、定容时水加多了 |
| D、定容时俯视刻度线 |
| m |
| M |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3- |
| B、酸性溶液中可能大量存在Na+、ClO-、SO42-、I- |
| C、常温下在c(H+)=1×10-13 mol?L-1的溶液中能大量存在Mg2+、Cu2+、SO42-、NO3- |
| D、加入铝粉能产生氢气的溶液中大量存在NH4+、Fe2+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用光亮洁净的铁丝蘸取某无色溶液,在无色灯焰上灼烧时观察到黄色火焰,则该溶液中一定含Na+,一定不含K+ |
| B、酸、碱中和反应的实质是H+与OH-结合生成水,故酸碱中和反应的离子反应都可用H++OH-=H2O来表示 |
| C、实验室常将硫磺撒在汞的表面,以除去不慎洒落的汞 |
| D、Na2O与Na2O2都能和水反应生成NaOH,所以它们都是碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
A、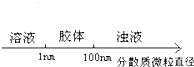 分散系的分类 |
B、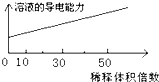 醋酸稀释 |
C、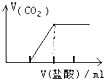 向Na2CO3溶液中逐滴滴入盐酸 |
D、 向AlCl3溶液中滴加过量的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用弱酸的电离平衡常数比较同温同物质的量浓度下强碱弱酸盐溶液的碱性强弱 |
| B、常温下pH=2的盐酸、氯化铵两种溶液中,水的电离程度相同 |
| C、用化学反应平衡常数推断该化学反应的剧烈程度 |
| D、将等体积、等pH的氢氧化钠溶液和氨水溶液分别稀释相同倍数,氨水的pH变化大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NO2、SO2、NO和SO3四种气体的物质的量浓度之比为1:1:1:1 |
| B、生成n molSO2同时有n mol SO3消耗 |
| C、K值不再发生变化 |
| D、密闭容器中气体的密度不再发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升温 | B、加压 |
| C、加水稀释 | D、滴加浓盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com