
实验室里有一瓶KCl与CaCl2的固体混合物,通过下面实验可确定该混合物中KCl和CaCl2的质量比,也可制得纯净的KCl,根据实验步骤填写下列空白:

(1)调整零点时,若指针偏向左边,应将左边的螺丝帽向(填左、右)______旋动。
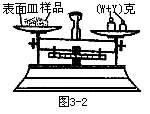
(2)某学生用已知质量y克的表面皿,准确称取W克样品,他在托盘天平的右盘放入(W+y)克砝码,在左盘的表面皿中加入样品,这时指针偏向右边,如图3-2示。
下面的操作应该是_______和______。
(3)加入的A是______,检验A是否过量的方法是______。

(4)过滤时,某学生的操作如图3-3所示,用文字说明图中的错误_____。
(5)滤液中加入的B物质是_______,应该加入过量B物质,理由是_____。
(6)为检验沉淀是否洗净,应在最后几滴洗出液中加入______,若______,表示沉淀已洗净。
(7)得到的固体C是_______。
(8)该混合物中KCl和CaCl2质量比的计算式是_____。
(9)配制100mL0.20mol·L-1的KCl溶液:某学生将准确称取的1.49gKCl固体放入烧杯中,加入约30mL蒸馏水,用玻璃棒搅拌使其溶解,将溶液由烧杯转移到100mL容量瓶中,然后往容量瓶中小心地加蒸馏水,直到液面接近标线2—3cm处,改用胶头滴管加蒸馏水,使溶液凹面最低点恰好与刻度相切,把容量瓶盖盖好,振荡摇匀,该学生操作中错误的是_____。
(1)右 (2)继续慢慢加入样品至天平指针指在标尺中间,称样完毕(3)K2CO3溶液,取上层清液少许,滴加盐酸,若有气泡产生,说明K2CO3过量 (4)一是玻璃棒未靠在滤纸上;二是漏斗底末端未靠在烧杯内壁上 (5)盐酸可使未反应的K2CO3完全转化为KCl (6)AgNO3溶液,无沉淀

本题是综合考查托盘天平的使用,过滤洗涤及物质的量浓度溶液的配制的基本操作技能。
(1)天平使用时应先调整零点,调整的方法是:若指针偏向左边时,说明天平左边重,应将左边的螺丝帽向右移动,直到指针指向中心为止。
(2)称量样品时,放好样品和砝码后,若指钍偏向右边时,说明此时右盘重,下面的操作应该继续慢慢加入样品至天平指针指在标尺中间,称样完毕。
(3)将样品溶于适量蒸馏水中,加入稍过量的K2CO3溶液,使样品中的CaCl2完全转化为CaCO3沉淀。化学方程式为
CaCl2+K2CO3====CaCO3↓+2KCl
检验K2CO3是否过量可用以下方法:取上层澄清液少许,滴加盐酸,若有气泡产生,说明K2CO3过量。</PGN0091A.TXT/PGN>
(4)图中的操作有两处错误:一是玻璃棒未靠在滤纸上,造成被滤液穿过滤纸与漏斗壁的间隙;二是漏斗底末端未靠在烧杯壁上,可能使滤液溅出。
(5)滤液中入的B物质是盐酸,盐酸过量可使未反应的K2CO3完全转化为KCl反应如下:
K2CO3+2HCl====2KCl+2H2O+CO2↑
(6)为检验沉淀是否洗净,应在最后的几滴洗出液中加入AgNO3溶液,若已将CaCO3沉淀洗涤净,洗出液中不再会含有Cl-,加入AgNO3溶液无沉淀生成,反之会有AgCl沉淀生成。
(7)过滤所得沉淀,洗涤后干燥,得固体C应是CaCO3。
(8)所得的CaCO3称其质量为W2g,由CaCl2和CaCO3的关系式可算出样品中CaCl2的量,设CaCl2为xg。
CaCO3 ~ CaCl2
100 111
W2 x
x=111W2/100(g)
前已称样品的总质量Wg又CaCl2的质量为111W2/100g所以KCl的质量为(W-111W2/100)g,则样品中KCl与CaCl2质量比为:
![]()
(9)有两处错误:一是烧杯中的溶液不能直接倒入容量瓶,而是沿玻璃棒倒入容量瓶;二是应该洗涤玻璃棒及烧杯2-3次,把洗涤转入容量瓶中。


科目:高中化学 来源:2001北京市海淀区高考模拟试卷 题型:058
实验室里有一瓶KCl与![]() 的固体混合物,通过下面实验可确定该混合物中KCl和
的固体混合物,通过下面实验可确定该混合物中KCl和![]() 的质量比,也可制得纯净的KCl,根据实验步骤填写下列空白:
的质量比,也可制得纯净的KCl,根据实验步骤填写下列空白:

(1)调整零点时,若指针偏向左边,应将左边的螺丝帽向(填左、右)________旋动.
(2)某学生用已知质量y g的表面皿,准确称取W g样品,他在托盘天平的右盘放入(W+y)g砝码,在左盘的表面皿中加入样品,这时指针偏向右边,如下图示.下面的操作应该是________和________.
(3)加入的A是________,检验A是否过量的方法是________.

(4)过滤时,某学生的操作如下图所示,用文字说明图中的错误________.

(5)滤液中加入的B物质是________,应该加入过量B物质,理由是________.
(6)为检验沉淀是否洗净,应在最后几滴洗出液中加入________,若________,表示沉淀已洗净.
(7)得到的固体C是________.
(8)该混合物中KCl和![]() 质量比的计算式是________.
质量比的计算式是________.
(9)配制100mL 0.20![]() 的KCl溶液:某学生将准确称取的1.49g
KCl固体放入烧杯中,加入约30mL蒸馏水,用玻璃棒搅拌使其溶解,将溶液由烧杯转移到100mL容量瓶中,然后往容量瓶中小心地加蒸馏水,直到液面接近标线2-3cm处,改用胶头滴管加蒸馏水,使溶液凹面最低点恰好与刻度相切,把容量瓶盖盖好,振荡摇匀,该学生操作中错误的是________.
的KCl溶液:某学生将准确称取的1.49g
KCl固体放入烧杯中,加入约30mL蒸馏水,用玻璃棒搅拌使其溶解,将溶液由烧杯转移到100mL容量瓶中,然后往容量瓶中小心地加蒸馏水,直到液面接近标线2-3cm处,改用胶头滴管加蒸馏水,使溶液凹面最低点恰好与刻度相切,把容量瓶盖盖好,振荡摇匀,该学生操作中错误的是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
(19分)实验室里有一瓶KCl与CaCl2的固体混合物,通过下面实验可确定该混合物中KCl和CaCl2的质量比,也可制得纯净的KCl,根据实验步骤填写下列空白:

 (1) 某学生用已知质量y克的表面皿,准确称取W克样品,他在托盘天平的右盘放入(W+y)克砝码,在左盘的表面皿中加入样品,这时指针偏向右边,如下图示。请补完整后面的操作是_______。
(1) 某学生用已知质量y克的表面皿,准确称取W克样品,他在托盘天平的右盘放入(W+y)克砝码,在左盘的表面皿中加入样品,这时指针偏向右边,如下图示。请补完整后面的操作是_______。
(2)滤液中加入的B物质是_______,应该加
入过量B物质,理由是_____。
(3)过滤得到沉淀C时,为检验沉淀是否洗净,
应用蒸馏水多次洗涤后,在最后几滴滤出
液中加入______,若______,表示沉淀已洗净。
(4)配制100mL0.20mol·L-1的KCl溶液:某学生用托盘天平将准确称取的(A)1.500gKCl固体放入烧杯中,加入(B)约30mL蒸馏水,用玻璃棒搅拌使其溶解,冷却到室温后,(C)将KCl溶液由烧杯小心倒入100mL容量瓶(不漏液)中,(D)然后往容量瓶中加蒸馏水,直到液面接近标线1—2cm处,摇匀并静置几分钟后,改用胶头滴管加蒸馏水,(E)使溶液凹面最低点恰好与刻度相切,把容量瓶盖盖好,振荡摇匀后装瓶。该学生操作中错误的是_____(填写编号)。
(5)下面哪些操作会导致所配的100mL0.20mol·L-1的KCl溶液浓度降低_________。
(A)容量瓶用蒸馏水洗涤三次直到洗净
(B)称量KCl固体时将砝码放在左盘
(C)未洗涤转移KCl溶液的烧杯
(D)转移KCl溶液时有KCl溶液溅出
(E)定容时仰视刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com