
| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(M) | n(N) | n(P) | ||
| ① | 500 | 0.3 | 0.2 | 0.3 |
| ② | 600 | 0.2 | 0.3 | 0.24 |
| ③ | 750 | 0.1 | 0.1 | x |
| A. | 实验①中,若5 min时测得n(N)=0.050 mol,则0~5min时间内平均反应速率v(P)=0.015 mo1/(L•min) | |
| B. | 实验②中达到平衡后,增大压强,M的转化率增大,平衡常数不变 | |
| C. | 600℃时该反应的平衡常数K=3.0 | |
| D. | 实验③中,达到平衡时,x<0.10 |
分析 A.实验①中,若5 min时测得n(N)=0.050 mol,此时生成P0.3mol,由此可计算反应速率;
B.增大压强,平衡不移动;
C.根据平衡时n(P)=0.24mol,可计算各物质的平衡浓度,以此可计算平衡常数;
D.对比①、②可知升高温度生成的P减少,说明平衡逆向移动,平衡常数减小,结合平衡常数计算.
解答 解:A.实验①中,若5 min时测得n(N)=0.050 mol,此时生成P0.3mol,则0~5min时间内平均反应速率v(P)=$\frac{\frac{0.3mol}{2L}}{5min}$=0.03mo1/(L•min),故A错误;
B.反应前后气体的体积相等,增大压强,平衡不移动,M的转化率不变,故B错误;
C.M (g)+N (g)?2P (g)+Q (s),
起始0.2mol 0.3mol
转化0.12mol 0.12mol 0.24mol
平衡0.08mol 0.18mol 0.24mol
则K=$\frac{(\frac{0.24}{2})^{2}}{(\frac{0.08}{2})×(\frac{0.18}{2})}$=4,故C错误;
D.对比①、②可知升高温度生成的P减少,说明平衡逆向移动,平衡常数减小,则实验③K<4,
则 M (g)+N (g)?2P (g)+Q (s),
起始0.1mol 0.1 mol
转化x x 2x
平衡0.1-x 0.1-x 2x
$\frac{{(2x)}^{2}}{(0.1-x)(0.1-x)}$<4,x<0.10,故D正确.
故选D.
点评 本题考查化学平衡有关计算及影响因素、反应速率有关计算等,为高考常见题型,侧重考查学生的分析能力和计算能力,注意把握平衡常数的计算以及应用,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ②④⑤ | C. | ②③④⑤ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

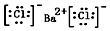 .
.| AgCl | AgI | Ag2CrO4 | |
| Ksp | 2×10-10 | 8.3×10-17 | 2×10-12 |
| 颜色 | 白 | 黄 | 砖红 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Cu(OH)2 | Mn(OH)2 |
| Ksp | 1.0×10-33 | 4.0×10-38 | 2.0×10-20 | 4.0×10-14 |
 ;“净化”时,加入(NH4)2S的作用为使Cu2+转化为CuS沉淀.
;“净化”时,加入(NH4)2S的作用为使Cu2+转化为CuS沉淀.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 构成原电池的条件有很多,其中一种就是利用电解质的浓度差构成“浓差电池”.当电解质中某离子的浓度越大时其氧化性或还原性越强.如图,甲池为3mol•L-1的AgNO3溶液,乙池为1mol•L-1的AgNO3溶液,A、B均为Ag电极.实验开始先闭合K2,断开K1,发现电流计指针发生偏转.下列说法不正确的是( )
构成原电池的条件有很多,其中一种就是利用电解质的浓度差构成“浓差电池”.当电解质中某离子的浓度越大时其氧化性或还原性越强.如图,甲池为3mol•L-1的AgNO3溶液,乙池为1mol•L-1的AgNO3溶液,A、B均为Ag电极.实验开始先闭合K2,断开K1,发现电流计指针发生偏转.下列说法不正确的是( )| A. | 一段时间后电流计指针将归零,此时可视为反应不再进行 | |
| B. | 当电流计指针归零后,闭合K1,断开K2后,乙池溶液浓度上升 | |
| C. | 当电流计指针归零后,闭合K1,断开K2后,乙中Ag电极质量增加 | |
| D. | 实验开始先闭合K2,断开K1,此时NO3-向B电极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
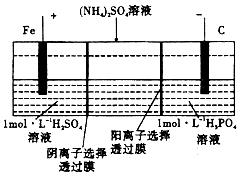
| A. | 阳极室溶液由无色变成浅绿色 | |
| B. | 当电路中通过lmol电子的电量时,阴极有0.5mol的气体生成 | |
| C. | 电解时中间室(NH4)2SO4溶液浓度下降 | |
| D. | 电解一段时间后,阴极室溶液中的溶质一定是(NH4)3PO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “可燃冰”被认为是21世纪新型洁净的能源,但大量开发和使用会诱发海底地质灾害,还会加重温室效应 | |
| B. | 碘元素被誉为“智力元素”,KI、KIO3、I2都可作碘盐的添加剂 | |
| C. | 硅橡胶无毒无味、耐高温又耐低温,可制成人造心脏,它属于无机非金属材料 | |
| D. | “雾霾天气”“温室效应”“光化学烟雾”的形成都与氮的氧化物无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
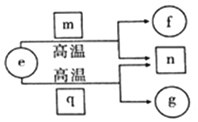 短周期元素X、Y、Z、W的原子序数依次增加,且Y、W为同主族元素.e、f、g分别是元素 Y、X、W的单质;m、n、q分别是由元素X、Y、W与元素Z组成的二元化合物,常温下的 状态依次为液态、气态、固态.上述物质的转化关系如图所示.下列说法错误的是( )
短周期元素X、Y、Z、W的原子序数依次增加,且Y、W为同主族元素.e、f、g分别是元素 Y、X、W的单质;m、n、q分别是由元素X、Y、W与元素Z组成的二元化合物,常温下的 状态依次为液态、气态、固态.上述物质的转化关系如图所示.下列说法错误的是( )| A. | 原子半径的大小:W>Z>X | |
| B. | 简单氢化物的沸点:W>Y>Z | |
| C. | 元素Y、Z、W形成的单质不止一种 | |
| D. | 元素Y、Z、W与元素X均能形成18e-的分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com