
【题目】下列实验操作会使最终结果偏高的是( )
A.配制![]() 溶液,定容时俯视刻度线
溶液,定容时俯视刻度线
B.用![]() 盐酸滴定
盐酸滴定![]() 溶液,起始读数时仰视
溶液,起始读数时仰视
C.用湿润的pH试纸测定![]() 溶液的pH
溶液的pH
D.测定中和热的数值时,将![]() 溶液倒入盐酸后,立即读数
溶液倒入盐酸后,立即读数
科目:高中化学 来源: 题型:
【题目】红磷P(s)和 Cl2 发生反应生成 PCl3 和 PCl5,反应过程和能量关系如图所示。△H 表示生成 1mol产物的焓变数据。下列热化学方程式不正确的是
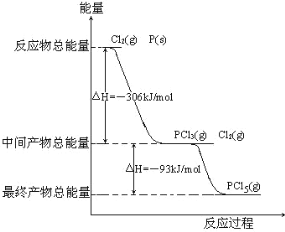
A.2P (s)+3Cl2 (g)=2PCl3 (g) △H=-612kJ·mol-1
B.PCl3 (g) =P (g)+ ![]() Cl2 (g) △H=306kJ·mol-1
Cl2 (g) △H=306kJ·mol-1
C.PCl5 (g)=PCl3 (g)+Cl2 (g) △H=93kJ·mol-1
D.2P (s)+5Cl2 (g)=2PCl5 (g) △H=-798kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸铁锂是制作电池的材料,其制备过程可以简化成如图所示。下列说法错误的是( )
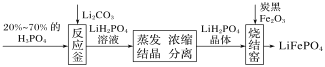
A.蒸发需要的硅酸盐材料仪器有:烧杯、酒精灯、玻璃棒、泥三角
B.反应釜中反应的化学方程式为2H3PO4+Li2CO3=2LiH2PO4+H2O+CO2↑
C.分离的操作是过滤
D.烧结窑中氧化铁与炭黑发生氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烟气研究组采用尿素H2N(CO)NH2溶液在50~700C时进行脱硫脱硝,装置如图所示。
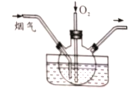
(1)如果不通入氧气,发现只有少量的烟气被吸收,生成对环境友好的物质。 被吸收的气体为___________ ;发生反应的化学方程式为__________________。
(2)如果通人烟气和一定量氧气的混合气,氮氧化物的吸收率仍然较低,可能的原因是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验淀粉水解的产物,设计如下实验方案:
![]()
请回答下列问题:
(1)试剂1为20%的H2SO4溶液,其作用是_________;
(2)试剂2为_________NaOH溶液,其作用是_________,使检验水解产物的实验得以顺利进行;发生反应的离子方程式为:_________;
(3)反应①的化学方程式为_________;
(4)为检验淀粉液是否已完全水解,取少量水解液于试管中,加入碘水,则证明淀粉未完全水解的现象是_________;
(5)如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的_________(填”能”或”否”)否,若不能,其原因是_________硫酸能溶解Cu(OH)2而使实验失败,最简单的改正措施是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒(Se)是第四周期ⅥA族元素,是人体内不可或缺的微量元素,其氢化物H2Se是制备新型光伏太阳能电池、半导体材料和金属硒化物的基础原料。
(1)已知:①2H2Se(g)+O2(g)![]() 2Se(s)+2H2O(l) ΔH1=a kJ·mol1
2Se(s)+2H2O(l) ΔH1=a kJ·mol1
②2H2(g)+O2(g)= 2H2O(l) ΔH2=b kJ·mol1
反应H2(g)+Se(s)![]() H2Se(g)的反应热ΔH3=___________kJ·mol1(用含a、b的代数式表示)。
H2Se(g)的反应热ΔH3=___________kJ·mol1(用含a、b的代数式表示)。
(2)T℃时,向一恒容密闭容器中加入3molH2和lmolSe,发生反应H2(g)+Se(s)![]() H2Se(g)。
H2Se(g)。
①下列情况可判断反应达到平衡状态的是___________(填字母)。
a.气体的密度不变 b.υ(H2)=υ(H2Se)
c.气体的压强不变 d.气体的平均摩尔质量不变
②当反应达到平衡后,将平衡混合气体通入气体液化分离器使H2Se气体转化为液体H2Se,并将分离出的H2再次通入发生反应的密闭容器中继续与Se反应时,Se的转化率会提高。请用化学平衡理论解释_________________________________。
③以5小时内得到的H2Se为产量指标,且温度、压强对H2Se产率的影响如下图所示:
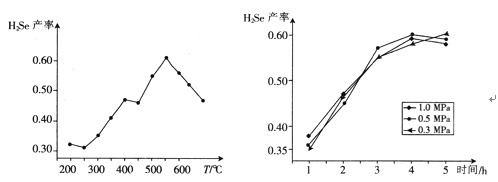
则制备H2Se的最佳温度和压强为______________________。
(3)已知常温下H2Se的电离平衡常数K1=1.3×104,K2=5.0×1011,则NaHSe溶液呈___________(填“酸性”或“碱性”),该溶液中的物料守恒关系式为____________________。
(4)用电化学方法制备H2Se的实验装置如下图所示:
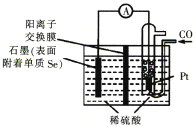
写出Pt电极上发生反应的电极反应式:_________________________________。
(5)H2Se在一定条件下可以制备CuSe,已知常温时CuSe的Ksp=7.9×1049,CuS的Ksp=1.3×1036,则反应CuS(s)+Se2-(aq)![]() CuSe(s)+S2-(aq)的化学平衡常数K=________(保留2位有效数字)。
CuSe(s)+S2-(aq)的化学平衡常数K=________(保留2位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨反应![]() N2(g)+
N2(g)+ ![]() H2(g)
H2(g) ![]() NH3(g) △H 的反应机理如图所示,图中“吸”表示各气态物质在催化剂表面吸附。下列说法错误的是
NH3(g) △H 的反应机理如图所示,图中“吸”表示各气态物质在催化剂表面吸附。下列说法错误的是
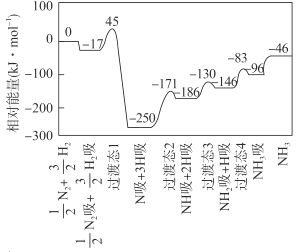
A.该反应的△H = -46 kJ·mol- 1
B.该反应机理中最大活化能为79 kJ·mol- 1
C.升高温度,该反应过渡态的能量会增大
D.该反应达到平衡后增大压强反应正向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2CO3溶液中滴加盐酸,反应过程中能量变化如下图所示,下列说法正确的是( )
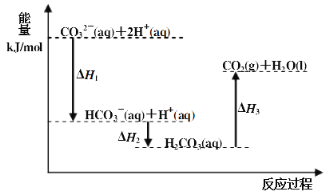
A.反应HCO3-(aq)+H+(aq)=CO2(g)+H2O(l) 为放热反应
B.CO32-(aq)+2H+(aq)=CO2(g)+H2O(l) H=(H1+H2+H3)
C.H1>H2 H2<H3
D.H2CO3(aq)=CO2(g)+H2O(l),若使用催化剂,则H3变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氢氧化钡是一种使用广泛的化学试剂。某课外小组通过下列实验测定某试样中Ba(OH)2·8H2O的含量。称取3.50g试样溶于蒸馏水配成100mL溶液,从中取出10.00mL溶液于锥形瓶中,加2滴指示剂,用0.1000mol/LHCl标准溶液滴定至终点,共消耗标准液20.00mL(杂质不与酸反应),求试样中氢氧化钡的物质的量为___;试样中Ba(OH)2·8H2O的质量分数为___。
(2)维尔纳配合物M是一种橙黄色单斜晶体,该晶体以浓氨水、双氧水、CoCl2·6H2O、NH4Cl为原料在加热条件下通过活性炭的催化来合成。为探究该晶体的组成,设计了如下图实验:
有一个步骤是氮的测定:准确称取一定量橙黄色晶体,加入适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品中的氨全部蒸出,用500.00mL7.0mol/L的盐酸溶液吸收,吸收结束后量取吸收液25.00mL,用2.00mol/L的NaOH溶液滴定过量的盐酸,终点消耗NaOH溶液12.50mL。
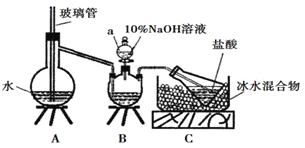
①上述装置A中,玻璃管的作用是__;
②装置A、B三脚架处应放置一个酒精灯作为热源,酒精灯应放置在__(填“A”或“B”)处。
③步骤一所称取的样品中含氮的质量为__g(计算结果保留2位有效数字)
④有同学提出装置C中所用盐酸的浓度过大易挥发,会造成测得氮的含量结果将__(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com