
【题目】为了检验淀粉的水解情况,某同学设计了以下三个实验方案,并根据实验现象,得出相应的结论:
甲:淀粉液![]() 水解液
水解液![]() 溶液变蓝 实验结论:淀粉未水解。
溶液变蓝 实验结论:淀粉未水解。
乙:淀粉液![]() 水解液
水解液![]() 无银镜现象 实验结论:淀粉未水解。
无银镜现象 实验结论:淀粉未水解。
丙:淀粉液![]() 水解液NaOH溶液,中和液
水解液NaOH溶液,中和液![]() 生成银镜 实验结论:淀粉完全水解。
生成银镜 实验结论:淀粉完全水解。
根据上述三个方案的操作及现象,首先回答结论是否正确,然后简要说明理由。如果三个结论均不正确,请另设计一个方案来证明淀粉已经水解完全了。
(1)方案甲:____________。
(2)方案乙:________。
(3)方案丙:___________。
(4)你的方案:________。
【答案】结论不正确;如果淀粉只是部分发生水解,未水解的淀粉遇碘也会变蓝色 结论不正确;淀粉发生水解生成葡萄糖,但由于水解液未用氢氧化钠溶液中和催化剂稀硫酸,无法与银氨溶液发生反应银镜反应 结论不正确;该实验只能证明淀粉已经水解,但不能证明淀粉完全水解 
【解析】
鉴别淀粉水解,加稀硫酸后加热,一段时间后,分为两份,一份加淀粉,变蓝,证明含有淀粉,但不能说没有水解,另一份先加氢氧化钠,再加银氨溶液,有银镜说明水解了,但不能说水解彻底,根据两份的现象综合分析才能说明淀粉的水解程度。
⑴水解液使碘水变蓝,只能说明存在淀粉,但是否已经水解不能证明,故答案为:结论不正确;如果淀粉只是部分发生水解,未水解的淀粉遇碘也会变蓝色。
⑵稀硫酸是该反应的催化剂,在反应中并未消耗,水解液为酸性,而银镜反应需在碱性溶液中进行,故答案为:结论不正确;淀粉发生水解生成葡萄糖,但由于水解液未用氢氧化钠溶液中和催化剂稀硫酸,无法与银氨溶液发生反应银镜反应。
⑶该实验只能说明淀粉已经水解,但是淀粉是否还存在,缺乏相关的现象验证,故该结论的证据不足,故答案为:结论不正确;该实验只能证明淀粉已经水解,但不能证明淀粉完全水解。
⑷为证明淀粉已经完全水解,可在丙方案的基础上添加以下实验步骤:取水解液,加入碘水、无明显现象,证明淀粉不存在,即可证明淀粉水解完全,故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】![]() (明矾),在生活、生产等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。
(明矾),在生活、生产等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。
![]()
回答下列问题:
(1)试剂①应选用________(填标号)
a.HCl溶液 b.![]() 溶液 c.氨水 d.NaOH溶液
溶液 c.氨水 d.NaOH溶液
写出有关反应的化学方程式________________________________。
(2)沉淀B的化学式为________,将少量明矾溶于水,溶液呈弱酸性,用方程式解释其原因________________________________。
(3)如果把废易拉罐先溶于过量的稀硫酸中,再加入过量的NaOH溶液,微热,过滤,得到的沉淀主要是________________________。
(4)在加入反应试剂时,为保证反应充分进行,往往加入的量要稍微过量。在操作2中如何检验沉淀完全,写出检验方法:________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用价电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,也可推测键角大小,下列判断正确的是( )
A.BF3与PCl3为三角锥形B.SO3与CO32-为平面三角形
C.SO2键角大于120oD.BF3是三角锥形分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三周期元素X、Y、Z、W的最高价氧化物溶于水可得四种溶液,0.01mol/L的这四种溶液pH与该元素原子半径的关系如下图所示。下列说法正确的是
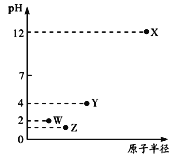
A. 简单离子半径: X>Y>Z>W
B. W的单质在常温下是黄绿色气体
C. 气态氢化物的稳定性: Z>W>Y
D. X和Y的最高价氧化物对应的水化物恰好中和时,溶液中的微粒共有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中实线是元素周期表的部分边界,其中上边界并未用实线标出。

根据信息回答下列问题:
(1)周期表中基态Ga原子的电子排布式为___。
(2)Fe元素位于周期表的___分区;Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为___。
(3)已知:原子数目和电子总数(或价电子总数)相同的微粒互为等电子体,等电子体具有相似的结构特征。与CO分子互为等电子体的分子和离子分别为___和___(填化学式)。在CO、CH3OH中,碳原子采取sp3杂化的分子有___。
(4)根据VSEPR理论预测ED4-离子的空间构型为___。B、C、D、E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的分子有__(任写2种化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】偏二甲肼[(CH3)2N—NH2]与 N2O4 是常用的火箭推进剂,火箭发射时常出现红棕色气体,发生的化学反应如下:
① (CH3)2N—NH2(1)+2N2O4(1) = 2CO2(g)+3N2(g)+4H2O(g) △H1<0
②N2O4(1) ![]() 2NO2(g) △H2>0
2NO2(g) △H2>0
下列说法不正确的是 ( )
A.反应①中,N2O4 为氧化剂
B.反应①中,生成1mo1CO2 时,转移16mo1e-
C.由反应②推断:加压、降温是获得液态 N2O4的条件
D.温度升高,反应①的化学反应速率减小、反应②的化学反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镧系为元素周期表中第ⅢB族、原子序数为57~71的元素。
(1)镝(Dy)的基态原子电子排布式为[Xe]4f106s2,画出镝(Dy)原子外围电子排布图:___________。
(2)高温超导材料镧钡铜氧化物中含有Cu3+,基态时Cu3+ 的电子排布式为________________。
(3)观察下面四种镧系元素的电离能数据,判断最有可能显示+3 价的元素是___________(填元素名称)。几种镧系元素的电离能(单位:kJ mol-1)
元素 | I1 | I2 | I3 | I4 |
Yb(镱) | 604 | 1217 | 4494 | 5014 |
Lu(镥) | 532 | 1390 | 4111 | 4987 |
La(镧) | 538 | 1067 | 1850 | 5419 |
Ce(铈) | 527 | 1047 | 1949 | 3547 |
(4)元素铈(Ce)可以形成配合物(NH4)2[Ce(NO3)6]。
①组成配合物的四种元素,电负性由大到小的顺序为________________(用元素符号表示)。
②写出氮的最简单气态氢化物水溶液中存在的氢键:__________________(任写一种)。
③元素Al 也有类似成键情况,气态氯化铝分子表示为(AlCl3)2,分子中Al 原子杂化方式为_____________,分子中所含化学键类型有______________(填字母)。
a.离子键 b.极性键 C.非极性键 d.配位键
(5)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中镨原子位于面心和顶点,则PrO2(二氧化镨)的晶胞中有________个氧原子;已知晶胞参数为a pm,密度为ρ g· cm-3,NA=_____________ (用含a、ρ的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予了锂离子电池开发的三位科学家。一种锂离子电池的反应式为LixC6+Li1﹣xCoO2![]() 6C+LiCoO2(x<1)其工作原理如图所示。下列说法不正确的是( )
6C+LiCoO2(x<1)其工作原理如图所示。下列说法不正确的是( )
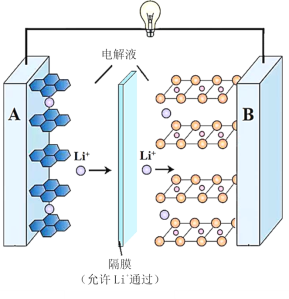
A.放电时A极电极式为:LixC6–xe-=6C+xLi+
B.放电时,若转移0.3mol电子,石墨电极将减重2.1g
C.充电时,A极接外电源的正极
D.该废旧电池进行“放电处理”有利于锂在B极回收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第四周期元素Q位于ds区,最外层电子半充满;短周期元素W、X、Y、Z第一电离能与原子序数的关系如下图所示,请回答下列问题(用Q、W、X、Y、Z所对应的元素符号作答):
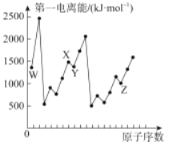
(1)基态Y原子核外共有___种运动状态不相同的电子。若用n表示能层,则与Y元素同族的元素的基态原子的价电子排布式为_________________。
(2)X、W组成的一种二元化合物常用作火箭燃料,该化合物中X原子的杂化方式为___________。该化合物常温下呈液态,其沸点高于Y2沸点的原因为___________。
(3)X2Y曾被用作麻醉剂,根据“等电子体原理”预测X2Y的空间构型为______________。
(4)XW3存在孤电子对,可形成[Q(XW3)4]2+离子,该离子中不存在_____________(填序号)。
A.极性共价键 B.非极性共价键 C.配位键 D.σ键 E.π键
(5)Q与X形成的一种二元化合物的立方晶胞结构如图所示:
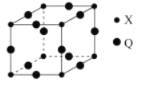
①Q原子周围距其距离最近的Q原子的数目为_______。
②该二元化合物的化学式为___________________。
(6)已知单质Q晶体的堆积方式为面心立方最密堆积,则单质Q晶体的晶胞中原子的空间利用率为_________________(用含π的式子表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com