
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源:不详 题型:单选题
| A.离子化合物的熔点一定比共价化合物的高 |
| B.二氧化碳分子中存在共价键和分子间作用力 |
| C.非极性键也可以存在于化合物中 |
| D.甲烷、氨和水都是由极性键结合而成的极性分子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
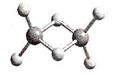
| A.Al2H6可以燃烧,产物为氧化铝和水 |
| B.1mol Al2H6中约含有4.8×1024个σ键 |
| C.60g Al2H6中含铝原子约为1.2×1023个 |
| D.Al2H6在固态时所形成的晶体是离子晶体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
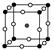
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
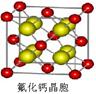
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
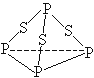
| A.分子中每个原子最外层均达到8电子稳定结构 |
| B.P4S3中硫元素为-2价磷元素为+3价 |
| C.热化学方程式为P4S3( s)+8O2(g)=P4O10(s )+3SO2(g)△H=-3677kJ/mol |
| D.一个P4S3分子中含有三个非极性共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
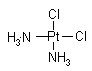 具有抗癌作用,而
具有抗癌作用,而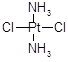 没抗癌作用。对此下列叙述正确的是( )
没抗癌作用。对此下列叙述正确的是( )| A.两者互为同分异构体,都是以Pt原子为中心的四面体结构 |
| B.两者互为同分异构体,都是以Pt原子为中心的平面结构 |
| C.两者为同一物质,都是以Pt原子为中心的四面体结构 |
| D.两者为同一物质,都是以Pt原子为中心的平面结构 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
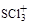 、SO2、SO32-、SO42-等。
、SO2、SO32-、SO42-等。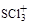 中S原子的轨道杂化类型是 ,
中S原子的轨道杂化类型是 ,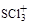 的空间构型是 。
的空间构型是 。| A.共价键 | B.氢键 | C.离子键 | D.配位键 E.分子间作用力 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com