
ijŠ£»ÆѧæĪĶāŠ”×éÓĆĮņĖįĢś·ĻŅŗ£Øŗ¬ÉŁĮæĮņĖįĶŗĶĻ”ĮņĖį£©£¬ÖʱøĮņĖįŃĒĢś¾§Ģå²¢½ųŠŠČēĻĀŹµŃ飮ÖʱøĮņĖįŃĒĢś¾§ĢåÖ÷ŅŖµÄ²Ł×÷Į÷³ĢČēĶ¼1
Ēėøł¾ŻĢāÄæŅŖĒó»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©AµÄ»ÆѧŹ½ĪŖ £®
£Ø2£©³ĆČČ¹żĀĖµÄÄæµÄŹĒ £®
£Ø3£©½į¾§²Ł×÷¹ż³ĢÖŠÓ¦æŲÖĘĀĖŅŗĖįŠŌµÄŌŅņŹĒ £®
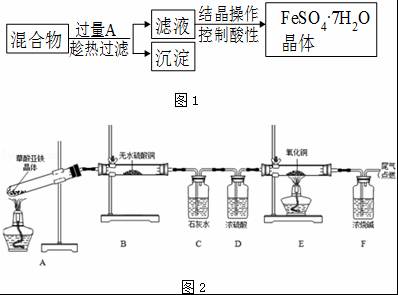
£Ø4£©ŹµŃéŹŅĄūÓĆĮņĖįŃĒĢśļ§ČÜŅŗ[£ØNH4£©2Fe£ØSO4£©2]ŗĶ²ŻĖįČÜŅŗ·“Ӧɜ³É²ŻĖįŃĒĢś£¬²ŻĖįŃĒĢś¾§Ģå£ØĻą¶Ō·Ö×ÓÖŹĮæ180£©ŹÜČČŅ×·Ö½ā£¬Ä³æĪĶāŠ”×éÉč¼ĘČēĶ¼2µÄŹµŃé×°ÖĆĄ“¼ģŃéĘä·Ö½ā²śĪļ£®
¢ŁøĆ×°ÖĆÖŠ×ī²»ŗĻĄķµÄ²æ·Ö £ØĢī×ÖÄø£©£¬ŌŅņŹĒ £®
¢ŚøÄÓĆÕżČ·×°ÖĆæŖŹ¼ŹµŃ飬B“¦±äĄ¶£¬ĖµĆ÷²ŻĖįŃĒĢś¾§ĢåÖŠÓŠ £»C“¦ÓŠ°×É«³Įµķ£¬E“¦ŗŚÉ«·ŪÄ©±äĪŖŗģÉ«£¬ĖµĆ÷²ŻĖįŃĒĢś·Ö½ā²śÉś £ØĢī»ÆѧŹ½£©£®
 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğø£½ØŹ”ÄĻĘ½ŹŠøßŅ»ĻĀѧʌµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ō¼Ę»®ŹµĻÖČ«ĒņĪĄŠĒĶØѶŠč·¢Éä77æÅĪĄŠĒ£¬ÕāÓėŅæ£ØIr£©ŌŖĖŲµÄŌ×ÓŗĖĶāµē×ÓŹżĒ”ŗĆĻąµČ£¬Ņņ“Ė³ĘĪŖ”°ŅæŠĒ¼Ę»®”±£®ŅŃÖŖŅæµÄŅ»ÖÖĶ¬Ī»ĖŲŹĒ19177Ir£¬ŌņĘäŗĖÄŚµÄÖŠ×ÓŹżÓėÖŹ×ÓŹżÖ®²īŹĒ£Ø £©
A. 77 B. 37 C. 191 D. 114
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½¶«Ź”ŃĢĢØŹŠøßŅ»ĻĀ3ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠø÷×éŌŖĖŲµÄŠŌÖŹµŻ±äĒéæö“ķĪóµÄŹĒ£Ø £©
A. N”¢O”¢FŌ×Ó×īĶā²ćµē×ÓŹżŅĄ“ĪŌö¼Ó
B. N”¢O”¢FŌ×Ó°ė¾¶ŅĄ“ĪŌö“ó
C. Na”¢Mg”¢AlŌŖĖŲ×īøßÕż»ÆŗĻ¼ŪŅĄ“ĪÉżøß
D. Li”¢Na”¢KµÄ½šŹōŠŌŅĄ“ĪŌöĒæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½¶«Ź”ø߶žĻĀĘŚ6ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚŗćČŻĆܱÕČŻĘ÷ÖŠ½ųŠŠN2£«3H2 2NH3·“Ó¦£¬ĘšŹ¼Ź±N2ŗĶH2·Ö±šĪŖ10 mol ŗĶ30 mol£¬µ±“ļµ½Ę½ŗāŹ±£¬N2µÄ×Ŗ»ÆĀŹĪŖ30%”£ČōŅŌNH3×÷ĪŖĘšŹ¼·“Ó¦Īļ£¬·“Ó¦Ģõ¼žÓėÉĻŹö·“Ó¦ĻąĶ¬Ź±£¬ŅŖŹ¹Ęä·“Ó¦“ļµ½Ę½ŗāŹ±ø÷×é³É³É·ÖµÄĪļÖŹµÄĮæ·ÖŹżÓėĒ°ÕßĻąĶ¬£¬ŌņNH3µÄĘšŹ¼ĪļÖŹµÄĮæŗĶĖüµÄ×Ŗ»ÆĀŹÕżČ·µÄŹĒ
2NH3·“Ó¦£¬ĘšŹ¼Ź±N2ŗĶH2·Ö±šĪŖ10 mol ŗĶ30 mol£¬µ±“ļµ½Ę½ŗāŹ±£¬N2µÄ×Ŗ»ÆĀŹĪŖ30%”£ČōŅŌNH3×÷ĪŖĘšŹ¼·“Ó¦Īļ£¬·“Ó¦Ģõ¼žÓėÉĻŹö·“Ó¦ĻąĶ¬Ź±£¬ŅŖŹ¹Ęä·“Ó¦“ļµ½Ę½ŗāŹ±ø÷×é³É³É·ÖµÄĪļÖŹµÄĮæ·ÖŹżÓėĒ°ÕßĻąĶ¬£¬ŌņNH3µÄĘšŹ¼ĪļÖŹµÄĮæŗĶĖüµÄ×Ŗ»ÆĀŹÕżČ·µÄŹĒ
A£®40 mol 35% B£®20 mol 30%
C£®20 mol 70% D£®10 mol 50%
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½¶«Ź”ø߶žĻĀĘŚ6ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ·“Ó¦ŌĄķ»ņ¹ż³Ģ£¬²»ÄÜÓĆĄÕĻÄĢŲĮŠŌĄķ½āŹĶµÄŹĒ
A£®ÓĆN2ŗĶH2ŗĻ³É°±Šč²ÉÓĆøßŃ¹”£
B£®ÓÉH2O2ÖĘŃõĘųŹ±Ź¹ÓĆMnO2“߻ƼĮ”£
C£®“×ĖįČÜŅŗ¼ÓĖ®Ļ”ŹĶ“×ĖįµÄµēĄė¶ČŌö“ó
D£®ĪĀ¶ČÉżøßĖ®µÄµēĄė³Ģ¶ČŌö“ó”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģŗÓÄĻŹ”ČżĆÅĻæŹŠøßČżÉĻµŚĖÄ“ĪÖŹ¼ģ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ±ķŹ¾¶ŌÓ¦»Æѧ·“Ó¦µÄĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ£Ø £©
A£®ĻņĻ”HNO3ÖŠµĪ¼ÓNa2SO3ČÜŅŗ£ŗSO32©+2H+=SO2”ü+H2O
B£®ĘÆ°×·ŪČÜŅŗÖŠĶØČė×ćĮ涞Ńõ»ÆĮņĘųĢå£ŗClO©+SO2+H2OØTHClO+HSO3-
C£®NaHCO3ČÜŅŗÖŠ¼ÓÉŁĮæBa£ØOH£©2ČÜŅŗ£ŗHCO3©+Ba2++OH©ØTBaCO3”ż+H2O
D£®ĻņCuSO4ČÜŅŗÖŠ¼ÓČėNa2O2£ŗ2 Na2O2+2Cu2++2H2OØT4Na++2Cu£ØOH£©2”ż+O2”ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģŗÓÄĻŹ”ČżĆÅĻæŹŠøßČżÉĻµŚĖÄ“ĪÖŹ¼ģ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ijĄė×Ó·“Ó¦ÖŠÉę¼°H2O”¢ClO?”¢NH4+”¢H+”¢N2”¢Cl©ĮłÖÖĪ¢Į££®ĘäÖŠN2µÄĪļÖŹµÄĮæĖꏱ¼ä±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£®ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø £©

A£®øĆ·“Ó¦µÄ»¹Ō¼ĮŹĒCl©
B£®ĻūŗÄ1 mol»¹Ō¼Į£¬×ŖŅĘ6 molµē×Ó
C£®Ńõ»Æ¼ĮÓė»¹Ō¼ĮµÄĪļÖŹµÄĮæÖ®±ČĪŖ2£ŗ3
D£®·“Ó¦ŗóČÜŅŗµÄĖįŠŌĆ÷ĻŌŌöĒæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģ¹ć¶«Ź”¹ćÖŻŹŠøßČżĻĀ4ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
½«4.6g½šŹōÄĘĶ¶Čėµ½95.6gĖ®ÖŠ£¬µĆµ½µÄČÜŅŗČÜÖŹµÄÖŹĮæ·ÖŹżŹĒ£Ø £©
A£®4.6% B£®7.6% C£®8% D£®10%
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½¶«Ź”ŃĢĢØŹŠø߶ž»ÆѧÉĻѧʌ¶Īæ¼ŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŦæŪµē³ŲµÄĮ½¼«²ÄĮĻ·Ö±šĪŖŠæŗĶŃõ»ÆŅų£¬µē½āÖŹČÜŅŗĪŖKOHČÜŅŗ£®·ÅµēŹ±Į½øöµē¼«·“Ó¦·Ö±šĪŖ£ŗZn+2OH©”śZn£ØOH£©2+2e©Ag2O+H2O+2e©”ś2Ag+2OH©ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®ČÜŅŗÖŠOH©ĻņÕż¼«ŅĘ¶Æ£¬K+”¢H+Ļņøŗ¼«ŅʶÆ
B£®Šæ·¢Éś»¹Ō·½Ó¦£¬Ńõ»ÆŅų·¢Éś»¹Ō·“Ó¦
C£®ŠæŹĒøŗ¼«£¬Ńõ»ÆŅųŹĒÕż¼«
D£®ŌŚµē³Ų·Åµē¹ż³ĢÖŠ£¬µē½āÖŹČÜŅŗµÄĖį¼īŠŌ»ł±¾±£³Ö²»±ä
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com