
| A. | ①③④ | B. | ②⑤⑥ | C. | ①②④⑤ | D. | ②④⑤⑥ |
分析 ①②③⑥都具有还原性,在空气中易被氧化,④可与空气中二氧化碳反应生成碳酸钙沉淀,⑤氯水含有次氯酸,在空气中次氯酸分解,以此解答该题.
解答 解:①H2S在空气被氧化生成S,溶液酸性降低,pH增大;
②H2SO3在空气中被氧化生成H2SO4,溶液酸性增强,pH减小;
③Na2S水解呈碱性,在空气中被氧化生成硫,同时生成NaOH,溶液碱性增强,pH增大;
④氢氧化钙与空气中二氧化碳反应生成碳酸钙沉淀,溶液碱性减弱,pH减小;
⑤氯水含有次氯酸,在空气中次氯酸分解生成盐酸,溶液酸性增强,pH减小;
⑥Na2SO3水解呈碱性,在空气中被氧化生成硫酸钠,溶液pH减小.
则减小的有②④⑤⑥.
故选D.
点评 本题考查较为综合,涉及元素化合物知识的综合应用,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意把握相关物质的性质,学习中注意相关基础知识的积累.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:选择题
| A. | 无色透明的水溶液中:K+、Ba2+、Cu2+、I- | |
| B. | 含有大量H+的水溶液中:NH4+、Fe2+、SO42-、MnO4- | |
| C. | c(HCO3-)=0.1mol/L的溶液中:Na+、K+、CO32-、Br- | |
| D. | 强碱性溶液中:Cl-、SO32-、HSO3-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向100mL 0.1mol/L的FeSO4溶液中,加入0.01mol Na2O2固体2Fe2++2Na2O2+2H2O═4Na++2Fe(OH)2+O2↑ | |
| B. | 向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全2Al3++3 SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| C. | 苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-?2C6H5OH+CO32- | |
| D. | 向20mL0.5mol/LFeBr2溶液中通入448mLCl2(标准状况):2Fe2++4Br-+3Cl2═2Fe3++6Cl-+2Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.84 mol•L-1 | B. | 18.4 mol•L-1 | C. | 0.184 mol•L-1 | D. | 0.018 4 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色酸性溶液中:Al3+、Cl-、Fe3+、SO42- | |
| B. | 在pH=0的溶液中:Fe2+、Mg2+、SO42-、NO3- | |
| C. | 0.1mol•L-1NaHCO3溶液中:K+、AlO2-、Cl-、NO3- | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:Fe3+、Ca2+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③⑥ | C. | ②④ | D. | ⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
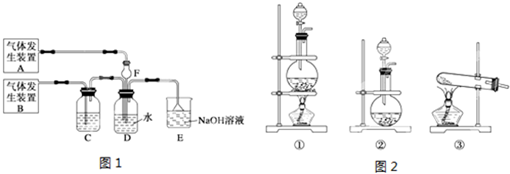
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图所示的ECC水泥是最新研制出来的,其最明显的特征是可以在弯曲状态下承受相当大的压力,因为材料里面有特殊制成的聚合体纤维微粒,所以ECC水泥可以在承受较大压力的状态下弯曲而不破裂.则聚合体纤维微粒在该材料中的作用是( )
如图所示的ECC水泥是最新研制出来的,其最明显的特征是可以在弯曲状态下承受相当大的压力,因为材料里面有特殊制成的聚合体纤维微粒,所以ECC水泥可以在承受较大压力的状态下弯曲而不破裂.则聚合体纤维微粒在该材料中的作用是( )| A. | 做粘合剂,起粘合作用 | B. | 做增强体,起骨架作用 | ||
| C. | 做导电体,起导电作用 | D. | 做原子晶体,起耐热作用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com