
分析 n(C2H5OH)=$\frac{4.6g}{46g/mol}$=0.1mol,完全燃烧生成二氧化碳和液态水放出热量136kJ,发生C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(l),可计算1mol甲醇燃烧放出的热量,并以此书写热化学方程式.
解答 解:n(C2H5OH)=$\frac{4.6g}{46g/mol}$=0.1mol,
所以1mol液态乙醇完全燃烧生成二氧化碳和液态水放出热量为136kJ•mol×0.1mol×10=1360kJ,
热化学方程式为C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(l)△H=-1360KJ/mol,
乙醇的燃烧热为1360KJ/mol,
故答案为:C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(l)△H=-1360KJ/mol;1360KJ/mol.
点评 本题主要考查了热化学方程式的书写,为高频考点,侧重考查学生的分析、计算能力,需要注意的有:物质的状态、反应热的数值与单位,反应热的数值与化学方程式前面的系数成正比,注意理解燃烧热的定义,题目难度不大.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:解答题
 氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法.
氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法.| 编号 | 温度/K | 反应时间/h | 反应物质的量配比 | 实验目的 |
| ① | 573 | 4 | 1:3 | 实验②和④探究温度对产率的影响 |
| ② | 573 | 4 | 1:4 | |
| ③ | 573 | 3 | 4:1 | 实验②和③探究反应时间对 产率的影响 |
| ④ | 673 | 4 | 1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油的分馏和煤的液化都是发生了物理变化 | |
| B. | 乙烯和乙炔都能与溴水发生加成反应且生成的产物相同 | |
| C. | 甲烷和氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型相同 | |
| D. | 苯能使酸性高锰酸钾溶液褪色,也能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
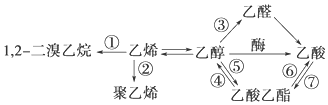
| A. | 反应①是加成反应 | B. | 只有反应②是加聚反应 | ||
| C. | 只有反应⑦是取代反应 | D. | 反应③是氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na2O是淡黄色固体,和水反应生成NaOH,是碱性氧化物 | |
| B. | 钠应保存于煤油中 | |
| C. | 钠投入滴有紫色石蕊试液的水中,溶液呈现红色 | |
| D. | 钠的焰色为黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com