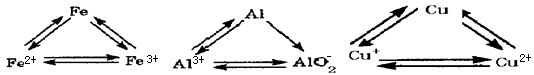
铝、铁、铜是人类生活和生产中具有广泛应用的三种金属单质,高中段的学习常把它们及化合物归结为重要的三角关系:
请回答下列问题
(1)氮化铝是一种性能良好的高温结构陶瓷,它的电子式:_________; 铁在周期表中的位置:_____________;
(2)铜生成铜绿是生活中常见的现象,其反应原理用方程式表示:_________; 氢氧化铝被称为两性氢氧化物,写出其酸式电离方程式:__________________;
(3)高铁酸盐被科学家们公认为绿色消毒剂, 它可以通过如下途径制备:次氯酸盐氧化法制备:采用次氯酸盐氧化法,在10.00 mL质量分数为8%的次氯酸钠溶液中加入5.5 g氢氧化钠和0.70 g硫酸铁,可制备摩尔浓度(物质的量浓度)为0.01 mol/L的高铁酸钠,写出制备的离子方程式: __________________高铁酸钠不仅可以消毒,也可以作净水剂,陈述理由:__________________
(4)燃料电池如图所示,写出石墨(I)电极上发生的电极反式:__________________ 。以此燃料电池作电源,以石墨为电极,电解一定浓度的CuSO4 溶液至无色后继续电解一段时间。断开电路,向溶液中加入0.1 mol Cu(OH)2,溶液恢复到电解之前的体积和浓度,则电解过程中转移电子的物质的量为_____________.。
(5)某研究性学习小组为探究铜、锌与浓盐酸反应,设计实验探究方案如下:实验用品:纯锌片、铜片、37%的浓盐酸、蒸馏水、氯化铜溶液实验记录:
背景资料:
某同学对实验中的白色沉淀进行分析,利用资料卡片资料①②大胆猜想,白色沉淀可能是CuCl。请你帮他设计验证方案。

 口算题天天练系列答案
口算题天天练系列答案