
【题目】下列图示与对应的叙述相符的是




甲 乙 丙 丁
A. 图甲表示常温下稀释pH均为11的MOH溶液和NOH溶液时pH的变化,由图可知溶液的碱性:MOH>NOH
B. 图乙表示常温下0.100 0 mol·L-1醋酸溶液滴定20.00 mL0.100 0 mol·L-1 NaOH溶液的滴定曲线
C. 图丙表示反应CH4(g)+H2O (g)![]() CO(g)+3H 2(g)的能量变化,使用催化剂可改变Eb﹣Ea的值
CO(g)+3H 2(g)的能量变化,使用催化剂可改变Eb﹣Ea的值
D. 图丁表示反应2CO(g)+2NO(g)![]() N2(g)+2CO2(g),在其他条件不变时,改变起始CO的物质的量,平衡时N2的体积分数变化,由图可知NO的转化率c>b>a
N2(g)+2CO2(g),在其他条件不变时,改变起始CO的物质的量,平衡时N2的体积分数变化,由图可知NO的转化率c>b>a
【答案】D
【解析】分析:本题考查对图像的理解和分析能力,涉及强弱电解质的稀释,中和滴定,能量变化和化学平衡。
详解:A、因为稀释能促进弱碱的电离,所以稀释pH均为11的MOH溶液和NOH溶液时pH变化大的碱性强,所以碱性:MOH<NOH,A错误;
B. 常温下0.100 0 mol·L-1醋酸溶液滴定20.00 mL0.100 0 mol·L-1 NaOH溶液,当加入20.00mL醋酸时,二者恰好反应生成醋酸钠,水解显碱性,而不是中性,所以B错误;
C.反应中加入催化剂会降低活化能,但不影响反应热,即使用催化剂不改变Eb﹣Ea的值,C错误;
D、反应2CO(g)+2NO(g)![]() N2(g)+2CO2(g),在其他条件不变的情况下增大起始物CO的物质的量,使一氧化氮转化率增大,NO的转化率c>b>a,D正确;因此本题答案为D。
N2(g)+2CO2(g),在其他条件不变的情况下增大起始物CO的物质的量,使一氧化氮转化率增大,NO的转化率c>b>a,D正确;因此本题答案为D。


科目:高中化学 来源: 题型:
【题目】工业上用含三价钒(V2O3)为主的某石煤为原料(含有Al2O3、CaO等杂质),钙化法焙烧制备V2O5,其流程如下:
![]()
【资料】:+5价钒在溶液中的主要存在形式与溶液pH的关系:
pH | 4~6 | 6~8 | 8~10 | 10~12 |
主要离子 | VO2+ | VO3 | V2O74 | VO43 |
(1)焙烧:向石煤中加生石灰焙烧,将V2O3转化为Ca(VO3)2的化学方程式是______。
(2)酸浸: ① Ca(VO3)2难溶于水,可溶于盐酸。若焙砂酸浸时溶液的pH=4,Ca(VO3)2溶于盐酸的离子方程式是______。
② 酸度对钒和铝的溶解量的影响如图所示:酸浸时溶液的酸度控制在大约3.2%,根据如图推测,酸浸时不选择更高酸度的原因是______。

(3)转沉:将浸出液中的钒转化为NH4VO3固体,其流程如下:
![]()
① 浸出液中加入石灰乳的作用是______。
② 已知CaCO3的溶解度小于Ca3(VO4)2。向Ca3(VO4)2沉淀中加入(NH4)2CO3溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:______。
③ 向(NH4)3VO4溶液中加入NH4Cl溶液,控制溶液的pH=7.5。当pH>8时,NH4VO3的产量明显降低,原因是______。
(4)测定产品中V2O5的纯度:
称取a g产品,先用硫酸溶解,得到(VO2)2SO4溶液。再加入b1 mL c1 mol·L1 (NH4)2Fe(SO4)2溶液(VO2+ + 2H+ + Fe2+ == VO2+ + Fe3+ + H2O)。最后用c2 mol·L1 KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2 mL。已知 MnO4被还原为Mn2+,假设杂质不参与反应。则产品中V2O5的质量分数是______。(V2O5的摩尔质量:182 g·mol1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中的颜色变化,与氧化还原反应无关的是
A | B | C | D | |
实验 | NaOH溶液滴入FeSO4溶液中 | 石蕊溶液滴入氯水中 | Na2S溶液滴入AgCl浊液中 | 热铜丝插入稀硝酸中 |
现象 | 产生白色沉淀,随后变为红褐色 | 溶液变红,随后迅速褪色 | 沉淀由白色逐渐变为黑色 | 产生无色气体,随后变为红棕色 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚氯乙烯(PVC)保鲜膜的安全问题引起广泛关注。PVC的安全隐患主要来自于塑料中残留的PVC单体以及不符合国家标准的增塑剂DEHA。工业上用乙烯和氯气为原料经下列各步合成PVC:
![]()
(1)乙是PVC的单体,其结构简式为_____________________;
(2)反应①的化学方程式为______________________________________________________;
(3)写出以下反应类型:反应②_________________;反应③_________________。
(4)邻苯二甲酸辛酯(DOP)是国家标准中允许使用的增塑剂之一,邻苯二甲酸( )是制造DOP的原料,它跟过量的甲醇反应能得到另一种增塑剂DMP(分子式为C10H10O4),DMP属于芳香酯,请写出DMP的结构简式为________________。
)是制造DOP的原料,它跟过量的甲醇反应能得到另一种增塑剂DMP(分子式为C10H10O4),DMP属于芳香酯,请写出DMP的结构简式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置或操作正确的是
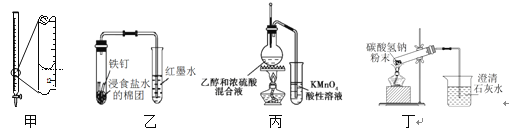
A. 装置甲液面读数为12.20 mL B. 装置乙可探究铁的吸氧腐蚀
C. 装置丙可检验乙烯的生成 D. 装置丁可验证碳酸氢钠受热分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤素指周期表中倒数第二列的元素,它们的化合物在生活生产中都有很重要的作用.氯化钾是临床常用的电解质平衡调节药,广泛用于临床各科,也常用于无机工业,是制造各种钾盐或碱如氢氧化钾、硫酸钾、硝酸钾、氯酸钾、红矾钾等的基本原料.
Ⅰ.老卤中主要含KCl和少量MgCl2、CaCl2、MgSO4等,需要分离提纯得到KCl.现有几种试剂:①盐酸;②K2CO3;③Na2CO3;④NaOH;⑤KOH;⑥Ba(OH)2;⑦BaCl2;⑧Ba(NO3)2 .
(1)为有效除去老卤中的杂质,加入试剂的合理顺序为_________.
A.先加NaOH,后加Na2CO3,再加BaCl2
B.先加BaCl2,后加NaOH,再加Na2CO3
C.先加K2CO3,后加KOH,再加Ba(NO3)2
D.先加Ba(NO3)2,后加K2CO3,再加KOH
E.先加Ba(OH)2,后加K2CO3
(2)过滤除去沉淀后还需要加入的试剂为______ (填序号),还需要进行的实验为_____.
A.蒸发结晶 B.降温结晶
Ⅱ.现有如下图仪器:

(1)仪器F的名称是_________.
(2)在实验室组成一套蒸馏装置肯定需要所给仪器中的一部分,按照实验仪器由下到上、从左到右的顺序,这些仪器依次是____________(填字母).
Ⅲ.小明同学将16.0 g NaOH固体溶于水配成100 mL溶液,其密度为1.60 g/mL,小明计划用配好的NaOH溶液制取简易消毒液。回答下列问题:
(1)用量筒取小明同学所配的NaOH溶液________ mL才能与标准状况下2.24 L氯气恰好完全反应.
(2)该消毒液即市面上的“84消毒液”,小明将(2)所取体积的NaOH溶液吸收好氯气后的溶液稀释到5 L使用,稀释后溶液中c(Na+)= ___________
(3)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员需要520 mL 2.3 mol/L的稀硫酸,拟采用98%(密度为1.84 g/cm3)的浓硫酸进行配制.
①需取用的浓硫酸的体积为________mL.
②取上述配好的硫酸溶液50 g与50 g 水混合,所得溶液的物质的量浓度________
A.等于1.15 mol/L B.小于2.30 mol/L 大于1.15 mol/L
C.小于1.15 mol/L D.大于2.30 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)除去NaNO3固体中混有的少量KNO3,所进行的实验操作依次为________、蒸发、结晶、________。
(2)除去KCl溶液中的SO![]() ,依次加入的溶液为(填溶质的化学式): ________________________。
,依次加入的溶液为(填溶质的化学式): ________________________。
(3)下列物质的分离和提纯方法操作为
①油水混合物________;
②自来水制备蒸馏水________;
③碘水中的I2________;
④KNO3溶液得到KNO3________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A. 铝片与盐酸反应Al+2H+===Al3++H2↑
B. 铝粉溶于烧碱溶液2Al+2OH-+2H2O ===2![]() +3H2↑
+3H2↑
C. 铝片放入硫酸铜溶液Al+Cu2+=== Al3++Cu
D. 镁条放入氯化铝溶液Mg+Al3+=== Mg2++Al
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是

A. 该硫酸的物质的量浓度为9.2mo1/L
B. 该硫酸与等体积的水混合所得溶液的质量分数为49%
C. 配制250mL 4.6mo1/L的稀硫酸需取该硫酸62.5mL
D. 该硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2mo1/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com