
| A. | Na2CO3和NaHCO3均可与NaOH溶液反应 | |
| B. | NaHCO3比Na2CO3热稳定性强 | |
| C. | 相同物质的量的Na2CO3和NaHCO3与足量盐酸作用时,产生的气体的量相同 | |
| D. | 相同质量的Na2CO3和NaHCO3与足量盐酸作用时,二者消耗的盐酸一样多 |
分析 A、Na2CO3与NaOH溶液不反应;
B、碳酸氢钠受热易分解;
C、根据碳守恒;
D、利用n=$\frac{m}{M}$,可计算物质的量,因酸足量,利用Na2CO3~CO2,NaHCO3~CO2来分析.
解答 解:A、Na2CO3与NaOH溶液不反应,而碳酸氢钠与氢氧化钠反应生成碳酸钠和水,故A错误;
B、碳酸氢钠受热易分解,不稳定,则热稳定性为Na2CO3>NaHCO3,故B错误;
C、相同物质的量的Na2CO3和NaHCO3与足量盐酸作用时,碳的物质的量相等,且全部转化为二氧化碳气体,所以产生的气体的量相同,故C正确;
D.设质量都是106g,则Na2CO3和NaHCO3的物质的量分别为1mol、$\frac{106}{84}$mol,根据Na2CO3~CO2,NaHCO3~CO2,产生的CO2的物质的量分别为1mol、$\frac{106}{84}$mol,故D正确;
故选:C.
点评 本题考查碳酸钠和碳酸氢钠的性质,涉及稳定性、与酸碱的反应等,注意与酸反应中量少的物质完全反应,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 通常状况下,2.24 L NO2和N2O4的混合气体中氮原子和氧原子数比为1:2 | |
| B. | 标准状况下,22.4 L己烷中共价键数目为19NA | |
| C. | 1 mol/L的Na2CO3溶液中所含阴离子数大于NA个 | |
| D. | 100 mL 0.3 mol/L 的硝酸溶液和200 mL 0.25 mol/L 的硫酸溶液混合配制成500 mL 混合溶液,则该溶液中的氢离子浓度为0.55 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 工业上用石灰对煤燃烧后形成的烟气进行脱硫,并能回收到石膏 | |
| C. | 单质硅可用于制半导体、光导纤维等 | |
| D. | 氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 被提纯的物质 | 杂质 | 除杂试剂 |
| A | FeCl3(aq) | Al3+(aq) | NaOH溶液、盐酸 |
| B | AlCl3(aq) | Cu2+ | Al粉 |
| C | NaHCO3(aq) | Na2CO3(aq) | CO2气体 |
| D | FeCl3(aq) | Cu2+ | Fe粉 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | Mg2+ | Cr3+ | Cl- |
| 浓度(mol/L) | 0.5 | 0.01 | a |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
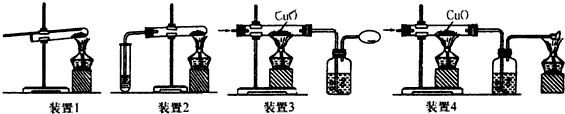
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铝溶液中滴加过量浓氨水:Al3++4OH-═AlO2-+2H2O | |
| B. | NaHCO3溶液水解:HCO3-+H2O═H2CO3+OH- | |
| C. | 浓氢氧化钠溶液吸收少量SO2气体:SO2+2OH-═SO32-+H2O | |
| D. | 向小苏打溶液中加入醋酸溶液:HCO3-+H+═CO2↑+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com