
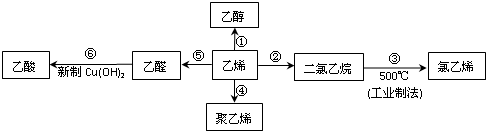
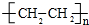 ,乙酸中的官能团为-COOH,名称为羧基,
,乙酸中的官能团为-COOH,名称为羧基,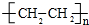 ;羧;
;羧;| 浓硫酸 |
| △ |
| △ |
| △ |


科目:高中化学 来源: 题型:
| A、υ(NH4)=0.8 mol/(L?s) |
| B、υ(O2)=1.0 mol/(L?s) |
| C、υ(NO)=1.0 mol/(L?s) |
| D、υ(H2O)=1.8 mol/(L?s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用带玻璃塞的试剂瓶保存Na2CO3溶液 |
| B、配制FeCl3溶液时,向溶液中加入少量铁粉和稀盐酸 |
| C、在铁件表面镀铜时,用铁件作阴极、铜作阳极、稀硫酸作电镀液 |
| D、实验室进行肥皂反应时,在油脂和氢氧化钠的混合液中加入适量酒精 |
查看答案和解析>>
科目:高中化学 来源: 题型:
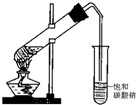

查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| CH3C≡CNa |

| 浓硫酸 |
| 170℃ |
| Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 电解质 | 平衡方程式 | 平衡常数K | Ksp |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.76×10-5 | - |
| C6H5OH(苯粉) | C5H5OH?C6H5O-+H+ | 1.1×10-10 | |
| NH3?H2O | NH3?H2O?NH4++OH- | 1.76×10-5 | - |
| BaSO4 | BaSO4(s)?Ba2++SO42-(aq) | - | 1.07×10-10 |
| BaCO3 | BaCO3(s)?Ba2++CO32-(aq) | - | 2.58×10-9 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com