
| 编号 | 实验操作 | 实验现象 | 结论及解释 |
| 1 | 分别取4种溶液,滴加紫色石蕊溶液 | 溶液变红的是①④溶液 | 略 |
| 2 | 向含酚酞的NaOH溶液中,各滴加等量的②③两种溶液 | ②中无明显现象 ③中红色明显变浅 | 滴加③时反应的化学方程式: C6H5OH+NaOH→C6H5ONa+H2O |
| 3 | 配制等物质的量浓度的CH3COONa、NaHCO3溶液,并比较其pH | NaHCO3溶液pH大于CH3COONa溶液 | 略 |
| 4 | 将CO2通入C6H5ONa溶液中 | 产生白色浑浊 | 反应的化学方程式:C6H5ONa+CO2+H2O=C6H5OH+NaHCO3 |
| 结论:4种物质的羟基中的氢原子的活泼性由强到弱的顺序是(填序号)④①③② | |||
分析 I.根据编号1实验可知 ①碳酸 ④乙酸显酸性能使石蕊变红,所以①碳酸 ④乙酸氢原子活泼性强于②乙醇 ③苯酚;
根据编号2实验可知苯酚具有弱酸性,可以和氢氧化钠反应,所以③苯酚 羟基氢原子活泼性强于②乙醇;
根据编号3实验可知乙酸酸性强于碳酸酸性,所以④乙酸中羟基氢原子活泼性强于①碳酸;
由实验1知碳酸酸性强于苯酚,所以将CO2通入C6H5ONa溶液中,生成苯酚;
II.根据实验目的,以及所发生的化学反应,确定实验方案的设计.
解答 解:I.本实验目的是比较不同物质的羟基中氢原子的活泼性,
通过实验1分别取4种溶液,滴加紫色石蕊溶液溶液变红的是①④溶液,可知①碳酸 ④乙酸氢原子活泼性强于②乙醇 ③苯酚;
通过实验2向含酚酞的NaOH溶液中,各滴加等量的②③两种溶液,②中无明显现象③中红色明显变浅,说明苯酚酸性能与氢氧化钠溶液发生酸碱中和反应方程式为:C6H5OH+NaOH→C6H5ONa+H2O,故③苯酚 羟基氢原子活泼性强于②乙醇;
通过实验3可确定④乙酸中羟基氢原子活泼性强于①碳酸;
通过实验4,将CO2通入C6H5ONa溶液中产生白色浑浊,苯酚钠和二氧化碳、水反应生成碳酸氢钠方程式为C6H5ONa+CO2+H2O=C6H5OH+NaHCO3,所以碳酸的酸性比苯酚强;
所以4种物质的羟基中的氢原子的活泼性由强到弱的顺序是乙酸、碳酸、苯酚、乙醇;
故答案为:C6H5OH+NaOH→C6H5ONa+H2O;产生白色浑浊;C6H5ONa+CO2+H2O=C6H5OH+NaHCO3;④①③②;
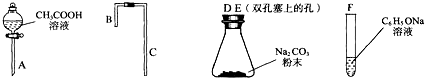
II.(1)一次比较乙酸、碳酸和苯酚的羟基中氢原子的活泼性,实验目的是证明酸性:乙酸>碳酸>苯酚.根据强酸制取弱酸的原则,须设计酸性:乙酸>碳酸>苯酚,即乙酸和碳酸钠反应生成二氧化碳(在A装置中),二氧化碳、水和苯酚钠反应生成苯酚和碳酸氢钠(在F装置中),
故答案为:D(或E);E(或D);F;
(2)在试管F之前增加了一个盛有饱和NaHCO3溶液的洗气装置,目的是将二氧化碳中的乙酸洗去,防止乙酸与苯酚钠反应,
故答案为:饱和NaHCO3.
点评 本题考查了性质方案的设计,题目难度中等,明确实验目的为解答关键,注意掌握性质方案设计与评价的原则,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:多选题
| A. | Na2CO3比NaHCO3易溶于水 | |
| B. | NaHCO3比Na2CO3稳定 | |
| C. | 澄清的石灰水能与Na2CO3反应,不与NaHCO3反应 | |
| D. | 等物质的量的Na2CO3和NaHCO3与等浓度足量的盐酸反应,消耗盐酸体积之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单氢化物的热稳定性:Z>W | B. | 最高价氧化物的水化物的酸性:X<Z | ||
| C. | 原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) | D. | 沸点:XW2>Y2W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
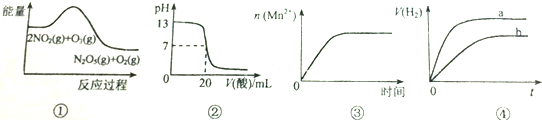
| A. | ①表示化学反应2NO2(g)+O3(g)═N2O5(g)+O2(g)△H>0 | |
| B. | ②表示25℃时,用0.5mol/LCH3COOH溶液滴定20mlNaOH溶液,溶液的pH随加入酸体积的变化 | |
| C. | ③表示10ml 0.01mol/L KMnO4 酸性溶液与过量的0.1mol/L H2C2O4溶液混合时,n(Mn2+) 随时间的变化 | |
| D. | ④表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 温度/℃ | N(B)/mol | N(D)/mol |
| T1 | 0.60 | - |
| T2 | - | 0.35 |
| A. | 上述信息可推知:T1<T2 | |
| B. | T1℃时,该反应的平衡常数K=$\frac{4}{9}$ | |
| C. | T2℃时,若反应达到平衡后再缩小容器的体积,c(C):c(D)不变 | |
| D. | T1℃时,若开始时反应物的用量均减小一半,平衡后A的转化率α(A)减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 洗净酸式滴定管后,立即装入标准盐酸进行滴定 | |
| B. | 锥形瓶用待测NaOH溶液润洗后,再装入NaOH 溶液进行滴定 | |
| C. | 操作过程中,滴定前平视读数,滴定后仰视读数 | |
| D. | 用酚酞作指示剂滴至红色刚退去,停止滴沄,立即读数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com