

| A.盐酸的浓度 | B.镁条的表面积 | C.Cl-的浓度 | D.溶液的温度 |
科目:高中化学 来源:不详 题型:单选题
A.N2(g)+3H2(g) 2NH3(g) △H<0 2NH3(g) △H<0 |
B.3O2(g) 2O3(g)△H>0 2O3(g)△H>0 |
C.H2(g)+I2(g) 2HI(g)△H<0 2HI(g)△H<0 |
D.NH4HCO3(s) NH3(g)+H2O(g)+CO2(g) △H>0 NH3(g)+H2O(g)+CO2(g) △H>0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.20℃,5 mL硫酸,2 mL水 | B.20℃,4 mL硫酸,3 mL水 |
| C.30℃,4 mL硫酸,3 mL水 | D.30℃,5 mL硫酸,2 mL水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 时间 酸 | 1 min | 2 min | 5 min | 15 min | 20 min |
| 3mol/L HCl | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
| 1.5mol/L H2SO4 | 均无明显现象(无气泡) | ||||
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.增加NH3浓度 | B.升高温度 | C.缩小体积增大压强 | D.降低温度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol·L-1FeCl3溶液 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
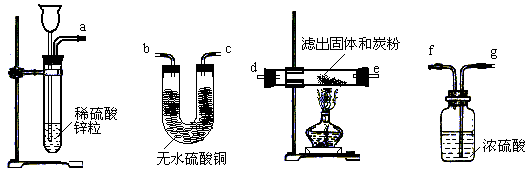
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
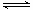 2SO3(g),能增大正反应速率的措施是( )
2SO3(g),能增大正反应速率的措施是( )| A.移去部分SO3 | B.增大容器的体积 |
| C.通入大量O2 | D.升高体系温度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
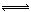 2SO3(g)当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
2SO3(g)当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。| 编号 | 改变的条件 | 生成SO3的速率 |
| ① | 升高温度 | |
| ② | 降低温度 | |
| ③ | 增大氧气的浓度 | |
| ④ | 使用催化剂 | |
| ⑤ | 压缩体积 | |
| ⑥ | 恒容下充人Ne | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com