
| A. | 己烷与溴的取代反应必须在光照条件下才能进行 | |
| B. | 氯乙烯聚合成聚氯乙烯塑料的本质是加成反应 | |
| C. | 苯与溴的取代反应的催化剂可以是FeBr3,也可以是Fe粉 | |
| D. | 溴乙烷的制取采取加成反应或取代反应的方法都一样 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
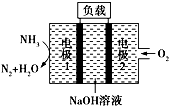
| A. | 电池工作时,电极2上发生氧化反应 | |
| B. | 电池工作一段时间后停止,溶液pH值比开始时明显增大 | |
| C. | 电极1发生的电极反应为2NH3+6OH--6e-═N2↑+6H2O | |
| D. | 用该电池做电源电解精炼铜,理论上每消耗0.2 mol NH3的同时阳极会得到19.2g纯铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
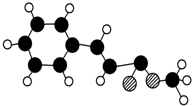 肉桂酸甲酯的球棍模型如图所示(图中球与球之间连线表示单键或双键).
肉桂酸甲酯的球棍模型如图所示(图中球与球之间连线表示单键或双键).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若X+和Y2-的核外电子层结构相同,则原子序数:X>Y | |
| B. | 元素周期表中位于金属和非金属分界线附近能找到半导体的元素 | |
| C. | Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH>Ba(OH)2 | |
| D. | 由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
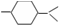 的分子中含有3个手性碳原子;
的分子中含有3个手性碳原子;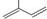 ;
;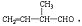 所含官能团的名称是碳碳双键、醛基;该有机物发生加成反应后,所得产物的结构简式为CH3CH2CH(CH3)CH2OH.
所含官能团的名称是碳碳双键、醛基;该有机物发生加成反应后,所得产物的结构简式为CH3CH2CH(CH3)CH2OH.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
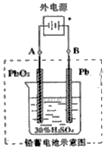 铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等.回答下列问题:
铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水果、蔬菜含有丰富的维生素,若要减肥,每天只吃水果蔬菜即可 | |
| B. | 米饭含有大量的淀粉,成人每天食用量不能超过100g | |
| C. | 要促进身体健康,各种饮食必须合理搭配 | |
| D. | 鸡蛋含丰富的蛋白质,人体所需蛋白质都可由鸡蛋提供,多吃有益 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com