
【题目】下列各组离子在溶液中能大量共存的是( )
A.Cu2+、K+、SO42-、NO3-B.Na+、H+、Cl-、HCO3-
C.Na+、NH4+、OH-、Cl-D.H+、K+、SO42-、CO32-
 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:
【题目】我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如图:
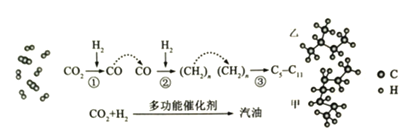
回答下列问题:
(1)二氧化碳分子中的化学键是______,物质乙的结构简式是______。
(2)写出反应![]() 的化学方程式______。
的化学方程式______。
(3)实验室常用纯净碳酸钙与稀盐酸反应制取二氧化碳气体,反应过程中产生二氧化碳的体积V(CO2)与时间关系如图:
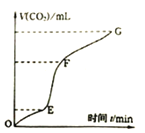
①由图象分析,化学反应速率最快一段是______。
②为了增大上述化学反应的反应速率,欲向溶液中加入下列物质或采取如下操作,你认为可行的是______![]() 填写序号
填写序号![]() 。
。
A.蒸馏水 B.氯化钠溶液 C.浓盐酸 D.加热
(4)二氧化碳能与氢氧化钠溶液反应,当二氧化碳与氢氧化钠反应的物质的量之比为2∶3时,溶液中的溶质是________。(填化学式)
(5)在一定条件下,工业上也可用CO2合成甲醇(CH3OH),其化学方程式为:CO2+3H2![]() CH3OH+H2O。将a molCO2与bmolH2充入容积为2L的密闭容器中发生上述反应,tmin时测得甲醇的物质的量为cmol。计算0-tmin内CO2的反应速率为______mol/(L·s)。[X的反应速率ν(X)=
CH3OH+H2O。将a molCO2与bmolH2充入容积为2L的密闭容器中发生上述反应,tmin时测得甲醇的物质的量为cmol。计算0-tmin内CO2的反应速率为______mol/(L·s)。[X的反应速率ν(X)=![]() ]
]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是( )
A. 放电时负极反应为Zn-2e-+2OH-===Zn(OH)2
B. 放电时正极反应为FeO42-+4H2O+3e-===Fe(OH)3+5OH-
C. 放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D. 放电时正极附近溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期主族元素,原子序数由A到E逐渐增大。①A元素最外层电子数是次外层电子数的2倍。②B的阴离子和C的阳离子与氖原子的电子层结构相同。③在通常状况下,B的单质是气体,0.1 mol B的气体与足量的氢气完全反应共有0.4 mol电子转移。④C的单质在点燃时与B的单质充分反应,生成淡黄色的固体,此淡黄色固体能与AB2反应可生成B的单质。⑤D的气态氢化物与其最高价含氧酸间能发生氧化还原反应。请回答下列问题:
(1)写出A元素的最高价氧化物的电子式_____________。
(2)B元素在周期表中的位置为_____________。
(3)B单质与C单质在点燃时反应的生成物中所含化学键类型有______________。
(4)D元素的低价氧化物与E的单质的水溶液反应的化学方程式为______________。
(5)C与D能形成2∶1的化合物,用电子式表示该化合物的形成过程______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
X | L层p电子数比s电子数多2个 |
Y | 第三周期元素的简单离子中半径最小 |
Z | L层有三个未成对电子 |
(1)写出元素X的离子结构示意图____________。
(2)写出Y元素最高价氧化物的水化物与NaOH溶液反应的离子方程式______________
(3)写出Y的价电子排布式_________________________。
(4)元素T与氯元素相比,非金属性较强的是_______(用元素符号表示),下列表述中能用于证明这一事实的是_______(填字母代号)。
A.气态氢化物的挥发性 B.两元素的电负性
C.含氧酸的酸性 D.氢化物中X—H键的键长(X代表T和Cl两种元素)
(5)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是___(填元素符号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①能量越低的物质就越稳定;②白磷转化成红磷是放热反应。据此判断下列说法中正确的是( )
A.在相同的条件下,红磷比白磷稳定
B.在相同的条件下,白磷比红磷稳定
C.红磷和白磷的结构相同
D.红磷容易发生自燃而白磷则不会自燃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是 ( )
A. 以石墨为电极电解MgCl2溶液:2Cl—+2H2O![]() Cl2+H2↑+2OH—
Cl2+H2↑+2OH—
B. CuC12溶液中加入氨水:Cu2++2OH- Cu(OH)2↓
C. KI溶液中滴入稀硫酸,空气中振荡:4H++4I-+O2 2I2+2H2O
D. 向NH4HCO3溶液中加过量的NaOH溶液并加热:NH![]() +OH-
+OH-![]() NH3↑+H2O
NH3↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A的结构简式为:![]()
(1)A的分子式为_____.
(2)A在NaOH水溶液中加热,经酸化得到有机物B和D,D是芳香族化合物.当有1mol A发生反应时,最多消耗_____mol NaOH.
(3)B在一定条件下发生酯化反应可生成某五元环酯,该五元环酯的结构简式为_____.
(4)写出苯环上只有一个取代基且属于酯类的D的所有同分异构体._____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:常温下甲胺(CH3NH2)的电离常数kb,pkb=-lgkb=3.4。CH3NH2+H2O![]() CH3NH3++OH-。下列说法不正确的是( )
CH3NH3++OH-。下列说法不正确的是( )
A. (CH3NH3)2SO4溶液中离子浓度:c(CH3NH3+)>c(SO42-)>c(H+)>c(OH-)
B. 常温下,pH=3的盐酸溶液和pH=11的CH3NH2溶液等体积混合,混合溶液呈酸性
C. 用标准浓度的盐酸滴定未知浓度的CH3NH2溶液的实验中,选择甲基橙作指示剂
D. 常温下向CH3NH2溶液滴加稀硫酸至c(CH3NH2)=c(CH3NH3+)时,溶液pH=10.6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com